Величина - ионный потенциал
Cтраница 2
В качестве показателей, определяющих природу ионов в растворе, приняты: для ионов главных подгрупп, лантаноидов, а также переходных элементов IV периода - электростатическая характеристика ( величина ионного потенциала pZ / r); для ионов побочных групп с 18-электронной структурой - ковалент-ная характеристика, равная разности между суммарным потенциалом ионизации ( /) и теплотой гидратации иона ( Я): / - Я. Именно эти характеристики наиболее полно отражают свойства ионов в растворах при их взаимодействии с другими ионами и молекулами. [16]
Таким образом, мы видим, что величина, соответствующая логарифму квадрата потенциала ионизации, умноженного на ионный радиус, гораздо лучше согласуется с аналитической классификацией ионов, чем величина ионного потенциала. [17]
В литературе встречаются различные названия величины / Сс; наиболее правильно называть ее коэффициентом равновесия, так как / Сс наряду с зависимостью от температуры, свойств ионитов, величины ионных потенциалов обменивающихся ионов зависит еще и от концентраций ионов. [18]
В литературе встречаются различные названия величины / Сс; наиболее правильно называть ее коэффициентом, равновесия, так как / Сс наряду с зависимостью от температуры, свойств ионитов, величины ионных потенциалов, обменивающихся ионов зависит еще и от концентраций ионов. [19]
Вода должна хемосорбироваться на всех указанных окислах аналогичным образом, но наименее прочно, в любой адсорбированной форме она будет удерживаться окисью цинка вследствие меньшей полярности ее кристаллической решетки. Величины ионных потенциалов свидетельствуют о том, что эти окислы имеют основной характер. [20]
Гидроксиды и оксиды простых катионов, которые растворимы в кислотах ( с образованием гидратированных катионов), а также в основаниях ( с образованием растворимых анионов), называются амфогперными ( см. разд. Для мягких катионов величина ионного потенциала не является достаточным критерием амфотерного поведения; гораздо более важную роль в этом отношении играют особенности электронного строения иона. Так, Sn2 с ионным потенциалом 1 82 образует вполне амфотерный гидроксид, в то время как Fe3 с ионным потенциалом 4 70 не дает гидроксидов с амфотерными свойствами. [21]
В табл. 4 показаны зависимости между величинами К ( логарифмические значения) и расположением катионов по аналитическим группам. При этом наблюдается значительно большее постоянство величин К, чем величин ионных потенциалов. [22]
Далее следует отметить что отвердевание системы возможно, если гидратообразование протекает с заметной скоростью, но не слишком большой. Разработаны оценочные методы выяснения влияния скоростей и интенсивности химического взаимодействия на образование структуры: по величине ионного потенциала; по отношению электроотрицательностей по Сандерсену; по тепловому эффекту реакции. Следовательно, имеется возможность прогнозировать оценку процесса по соответствию скоростей. [23]
Типичные окислы - изоляторы второго малого периода и пятиокись фосфора ( все они имеют конфигурацию катионов Is22s22pe) можно использовать для иллюстрации ряда поверхностных свойств. Эффективные ионные заряды гораздо меньше формальных зарядов, приведенных в таблице ( за исключением MgO), но формальные величины ионных потенциалов позволяют перекинуть мостик к более старым ионным теориям и некоторым полезным корреляциям, например к корреляции с тенденцией к стеклованию. [24]
Данные рис. 13, г, д свидетельствуют о том, что в поведении ионов редкоземельных элементов в растворе и фазе ионита имеется некоторая аналогия. Об этом свидетельствует одинаковый характер зависимости констант нестойкости по первой ступени сульфатных комплексов ( рК) и коэффициентов распределения этих ионов от величины ионного потенциала. [25]
Закономерное изменение электроотрицательностей в ряду В ( 2 0), А1 ( 1 5) и Са ( 1 0) частично объясняет то, что диссоциация борной кислоты происходит с отщеплением только одного протона, в то время как диссоциация гидроксида алюминия может происходить как с отщеплением протонов, так и с отщеплением гидроксид-иона, а диссоциация гидроксида кальция возможна только с отщеплением гидроксидных групп. Другим критерием, позволяющим судить о том, происходит ли в тех или иных соединениях при диссоциации отщепление гидроксидных групп, является величина ионного потенциала центрального атома ( см. разд. [26]
Кроме того, литий обнаруживает сходство с магнием по диагональному направлению в периодической системе, как это было отмечено еще Менделеевым, так же как бериллий с алюминием. Растворимость гидроокиси лития промежуточная по величине между растворимостями гидроокисей натрия и магния. По величине ионного потенциала литий занимает также промежуточное положение между катионами I и II групп. Ионы Li и Na образуют труднорастворимые цинк-уранил-ацетаты. [27]
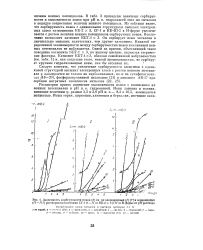 |
Зависимость сорбируемости ионов ( S из их азотнокислых ( / и сернокислых ( II-III растворов катионитами СГ-1 ( I-I1 и КБ-2 X 3 ( / / / в Н - форме от рН раствора. [28] |
Из таблицы видно, что сорбируемость ионов с одинаковыми структурами внешних электронных слоев катионитами КБ-2 X 3, СГ-1 и КБ-4П-2 в Н - форме увеличивается с ростом величин ионных потенциалов сорбируемых ионов. Он сорбирует ионы металлов в значительно меньших количествах, чем другие катиониты. Никакой определенной закономерности между сорбируемостью ионов и величиной ионных потенциалов не наблюдается. Одной из причин, объясняющей такое поведение катионита КБТ-1 X 3, по нашему мнению, являются стеричес-кие факторы. Катионит КБТ-1 ХЗ, обладая самой низкой набухаемостью ( см. табл. 1) и, как следствие этого, низкой проницаемостью, не сорбирует крупные гидролизованные ионы, как бы отсеивая их. [29]
Из табл. 9 - 5 также видно, что при данной структуре сила кислоты уменьшается по мере увеличения размера центрального атома. Эта закономерность была использована Картледжем при первых попытках найти зависимость между структурой кислоты и ее силой. Рассматривая кислоты и основания как гидроокиси соответственно неметаллов и металлов, Картледж показал, что решение - является ли гидроокись кислотой, основанием или амфотерным соединением - может быть принято на основании величины ионного потенциала Ф, представляющего собой отношение заряда центрального иона к его радиусу. По Карт-леджу, если ] / Ф 2 2, гидроокись является основанием, при 2 2 УФ 3 2 гидроокись амфотерна, а при УФ 3 2 - это кислота. [30]
Страницы: 1 2 3