Величина - ионизационный потенциал
Cтраница 2
Подставляя в эту формулу величины ионизационных потенциалов, видим, что электрон ионизирует газовые молекулы, когда скорость его движения свыше 1000 км / сек. [16]
В подгруппах аналогов изменение величин ионизационных потенциалов протекает закономерно, у s - f - и р - ( кроме подгруппы 3) элементов, а именно - сверху вниз ионизационный потенциал падает, так как радиусы атомов в этом направлении увеличиваются. В подгруппе бора имеет место поочередное падение и возрастание. В подгруппах с ( - элементов, кроме подгруппы 3В, ионизационные потенциалы уменьшаются снизу вверх в подгруппах 4В, 5В, 6В и в группе никеля, а в остальных наименьшее значение ионизационного потенциала характерно для среднего элемента. Чем меньше ионизационный потенциал, тем легче атом теряет свой электрон, переходя в положительный ион. [17]
Для бора и кислорода величины ионизационных потенциалов уменьшаются. Это объясняется тем, что отрыв одного непарного - электрона от атома бора происходит легче, чем s - электрона с заполненного s - подуровня атома бериллия. Точно также энергия отрыва одного парного р-электрона атома кислорода меньше энергии отрыва одного электрона с наполовину заполненного / о-подуровня атома азота. Отрыв электронов с полностью заполненного подуровня требует значительной энергии. [18]
Рассмотрение электронного строения атома, величины ионизационного потенциала, эффекта Холла и др. для щелочных металлов дает основание Хрущеву [65] сделать тот же вывод о сохранении ближнего порядка, соответствующего ОЦК-структуре. [19]
 |
Устройство газотрона ( а, его вольт-амперная характеристика ( б и условное обозначение газотрона в принципиальных схемах ( в, г. [20] |
Когда напряжение на аноде достигнет величины ионизационного потенциала U3, в газе в результате ударной ионизации возникнет разряд и ток резко увеличится. [21]
В этом же направлении уменьшается величина ионизационного потенциала. Атом лития отличается от других тем, что у него на уровне, соседнем с наружным, имеется два электрона, тогда как у других атомов по восемь. [22]
При наличии хотя бы ничтожных примесей величина ионизационного потенциала заметно изменяется. Этим пользуются для его снижения у низковольтных вентилей. [23]
 |
Кривая эффективных атомных радиусов простых веществ в зависимости от расположения элементов в периодической системе. [24] |
Если восстановительные свойства металла зависят от величины ионизационного потенциала, то окислительную способность неметалла характеризует так называемое сродство к электрону. [25]
От каких из перечисленных факторов зависит величина ионизационного потенциала атома химического элемента: радиус атома; атомная масса; заряд ядра атома; эффективный заряд ядра атома; структура внешнего электронного слоя атома; заселенность орбиталей внешнего слоя атома; эффект экранирования; порядковый номер элемента; положение элемента в Периодической системе. [26]
Для характеристики восстановительно-окислительных свойств нейтральных атомов пользуются величинами ионизационных потенциалов и сродства к электрону. [27]
 |
Строение и физические константы галогенов. [28] |
Совокупность его физических свойств: полиатомность молекул, величина ионизационного потенциала, электроотрицательность, газообразное агрегатное состояние и др. - позволяет относить его к галогенам. В этой подгруппе его к рассматривают. Однако у водорода есть ряд специфических свойств, отличных от галогенов, поэтому этот элемент и его соединения изучаются в конце главы. [29]
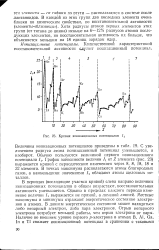 |
Кривая ионизационных потенциалов 1г. [30] |
Страницы: 1 2 3 4