Величина - ионизационный потенциал
Cтраница 3
В периодах ( восходящие участки кривой) слева направо величины ионизационных потенциалов в общем возрастают, восстановительная активность уменьшается. Однако в пределах каждого периода изменение величин Л выражается не прямой, а ломаной линией. Местные максимумы и минимумы отражают энергетическое состояние электронов в атомах. В даннсм энергетическом состоянии может находиться либо непарный электрон, либо пара электронов. [31]
В каких случаях сравнительная активность металлов может оцениваться по величинам ионизационных потенциалов их атомов и в каких случаях - по величинам нормальных потенциалов металлов. [32]
 |
Вольтампер-ная характеристика дуги с раскаленным катодом. [33] |
При аномальной низковольтной дуге переменное напряжение на аноде не достигает величины ионизационного потенциала, но в некоторые фазы колебания бывает больше наименьшего потенциала возбуждения газа. Точно так же случай аномальной дуги сводится к случаю нормальной, если в дуге существует специфическое распределение потенциала, при котором на некотором расстоянии от катода потенциал выше не только потенциала катода, но и потенциала анода. [34]
Прочность связи между ядром и электронами может быть измерена по величине ионизационного потенциала /) - энергии, которую надо затратить, чтобы удалить электрон из атома. [35]
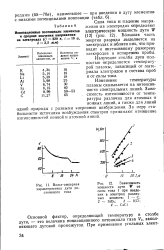 |
Вольт-амперная характеристика дуги постоянного тока.| Зависимость мощности дуги W от силы тока / при введении в электрод различных веществ. / - С. 2 - SiO2. 3 - КС1. 4 - CsCi. [36] |
Основной фактор, определяющий температуру в столбе дуги, - это величина ионизационного потенциала газа У -, заполняющего дуговой промежуток. [37]
В зависимости от величины критерия недостроенности d - электронной оболочки и величины ионизационного потенциала атома неметалла изменяется электронная концентрация между остовами атомов в решетке и характер ее распределения. [38]
О характере прочности связи электронов в атоме элемента можно судить по величине ионизационного потенциала, который показывает расход необходимой для отрыва одного электрона от нейтрального атома ( рис. 36) в электроновольтах ( эв) или ккал / г-атом. Легче всего теряют по валентному электрону атомы щелочных металлов, наибольшая затрата энергии требуется для отрыва электрона от атома инертных элементов, имеющих прочную электронную структуру. [39]
На рис. 2 показаны положения максимумов эффективного выхода отрицательных ионов для некоторых соединений вместе с величинами ионизационных потенциалов. Связь резонансных состояний с возбуждением ридберговских состояний молекул несомненна. [40]
Шишокин [118, 119] предложил метод расчета на основе линейной зависимости между энтальпией образования и квадратным корнем из величины ионизационного потенциала. [41]
Конечно, судить о прочности связей в соединениях инертных газов с другими элементами только на основании величин ионизационных потенциалов инертных газов - это очень упрощенный подход. Ведь, как уже говорилось, связь, например, в молекулах фторидов инертных газов преимущественно ковалентная. [42]
При заполнении внутренних подуровней у атомов d - элементов радиусы атомов колеблются незначительно, а потому и величины ионизационных потенциалов изменяются по отношению друг к другу сравнительно мало, хотя общее небольшое возрастание слева направо имеет место. [43]
Показано, что значения энергий активации диффузии бора, углерода и кремния в переходные металлы связаны с величиной ионизационного потенциала диффундирующего металлоида и степенью недостроенности rf - электронных подуровней переходных металлов и хорошо согласуются с физическими константами как переходных металлов, так и соответствующих боридных, карбидных и силицидных фаз. [44]
Какие из приведенных факторов влияют на положение металла в ряду напряжений: величина сродства к электрону атомов; величина ионизационного потенциала атомов; энергия кристаллической решетки металла; теплота гидратации ионов металла; концентрация ионов металла в растворе. [45]
Страницы: 1 2 3 4