Величина - произведение - растворимость - осадок
Cтраница 1
Величины произведения растворимости осадка и константы диссоциации соответствующей кислоты обычно известны; поэтому из уравнения ( 8) можно вычислить величину константы равновесия. [1]
Величины произведения растворимости осадка и константы диссоциации соответствующей кислоты обычно известны; поэтому из уравнения ( 8) можно вычислить величину константы равновесия. Несколько типичных задач рассматривается в приведенных ниже примерах. [2]
Если известна величина произведения растворимости осадка и константа кислотной диссоциации реактива, можно рассчитать растворимость осадка при различных значениях рН раствора. В этом отношении органические реактивы во многом аналогичны сероводороду. Осадок диметилглиоксимата никеля очень мало растворим, величина его произведения растворимости составляет 2 3 - 10 - 25, но этот осадок, так же как сульфид никеля или сульфид железа, не выпадает из сильно кислых растворов. [3]
Растворимость труднорастворимых соединений зависит от величины произведения растворимости осадка. [4]
Часть осаждаемых ионов, соответствующая величине произведения растворимости осадка, всегда остается в растворе. Но, как и в качественном анализе, нас интересует, конечно, не теоретическая, а практическая полнота осаждения. В качественном анализе мы могли назвать осаждение какого-либо иона практически полным в тех случаях, когда остающиеся в растворе количества его настолько малы, что никаким дальнейшим операциям анализа помешать уже не могут. [5]
Часть осаждаемых ионов, соответствующая величине произведения растворимости осадка, всегда остается в растворе. Но, как и в качественном анализе, нас интересует, конечно, не теоретическая, а практическая полнота осаждения. В качественном анализе мы могли назвать осаждение какого-либо иона практически полным в тех случаях, когда остающиеся в, растворе количества его настолько малы, что никаким дальнейшим операциям анализа помешать уже не могут. [6]
Правило произведения растворимости не только подчеркивает значение величины произведения растворимости осадка в процессах осаждения, ной позволяет также наметить те меры, при помощи которых недостаточно полное осаждение можно сделать практически полным. [7]
Растворимость труднорастворимых соединений в различных растворителях зависит от величины произведения растворимости осадка. 1ЫО-ЗЙ; ПРСг ( он: - 5 4 - 10 - 31 и ПРА1 ( он), 1 9 - 10 - 33), в солях аммония не растворяются. [8]
Математическое исследование вопроса показывает, однако, что если величина произведения растворимости осадка мала, а величина К соответствующей слабой кислоты во много раз больше величины К. [9]
Математическое исследование вопроса показывает, однако, что если величина произведения растворимости осадка мала, а величина К. [10]
Большая или меньшая полнота осаждения определяется в первую очередь величиной произведения растворимости осадка. Но указанная величина постоянна только при неизменной температуре. Если же температура изменяется, то изменяется и величина произведения растворимости осадка. [11]
Следует заметить, что рассмотренные выше расчеты кривых титрования по величине произведения растворимости осадка являются лишь приближенными. В действительности дело значительно осложняется явлениями адсорбции ( соосаждения), влияние которых не учтено при расчете. [12]
 |
Кривая титрования 0 1 н. [13] |
Кроме этих двух факторов скачок на кривой титрования зависит также от величины произведения растворимости осадка. [14]
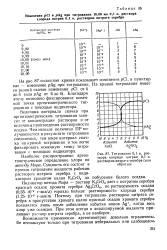 |
Титрование 0 1 н. рас. [15] |
Страницы: 1 2 3