Величина - ионный радиус
Cтраница 2
В силу сходства величин ионных радиусов для одинаковых видов ионов актиноидов образуются в большинстве случаев изо-структурные соединения. [16]
Все данные по величинам ионных радиусов взяты из книги Г. Б. Бокия: Введение в кристаллохимию ( Изд-во МГУ. [17]
Устойчивая трехвалентность иттрия, величина ионного радиуса и полный изоморфизм его с лантанидами иттриевой подгруппы легко объясняют тот факт, что иттрий не образует самостоятельных минералов. Он встречается исключительно в тех минералах, в которых имеются лантаниды иттриевой подгруппы ( от Gd до Lu), причем превалирует над ними так же, как церий над элементами цериевой подгруппы. [18]
Устойчивая трехпалептпость пттрия, величина ионного радиуса и полный изоморфизм его с лантанидами иттриевой подгруппы легко объясняют тот факт, что иттрий не образует самостоятельных минералов. Он встречается исключительно в тех минералах, в которых имеются лантаниды иттриевой подгруппы ( от Gd до Lu), причем превалирует над ними так же, как церий над элементами цериевой подгруппы. [19]
В табл. 17 приведены величины ионных радиусов по Г. Б. Вокию И Н. В. Белову. Под символом элемента в каждой клетке периодической таблицы выписаны ионные радиусы в ангстремах для случаев разной валентности. [20]
Таким образом, влияние величины ионного радиуса Ме2 на структуру расплава, и прежде всего на его вязкость, является двойственным и зависит от преобладания какой-либо из этих сторон, а следовательно, тесно связано с составом расплава и дозировкой добавки. [21]
Равенство зарядов, близость величин ионных радиусов и, наконец, аналогия электронных структур трансурановых ионов и лантаноидов являются предпосылками к близости свойств этих элементов в комплексах. [22]
Связь вяжущих свойств с величиной эффективного ионного радиуса отражает тонкую структуру рассматриваемых соединений. Изменение радиуса иона приводит к изменению типь кристаллической решетки и тем самым к изменению свойств. [23]
По ряду своих свойств ( величине ионного радиуса, растворимости солей, основности) иттрий похож на элементы иттриевой подгруппы. Скандий, хотя и близок по своим свойствам РЗЭ, но в меньшей степени, чем иттрий. [24]
Для таких структур важное значение имеют величины ионных радиусов элементов, определяющие геометрические пределы устойчивости структур с различными координационными числами. [25]
Приводимые в этом параграфе и далее величины эффективных ионных радиусов определены, исходя из характеризующихся координационным числом 6 структур типа NaCl, причем за основу брались соединения, в которых взаимное влияние химической природы ионов должно быть минимальным. [26]
Приводимые в этом параграфе и далее величины эффективных ионных радиусов определены исходя из характеризующихся координационным числом 6 структур типа NaCl, причем за основу брались соединения, в которых взаимное влияние химической природы ионов должно быть минимальным. [27]
Изменение энтропии AS0 не коррелируется с величинами гидрати-рованных ионных радиусов, однако оно линейно растет с увеличением радиуса иона как такового. Согласно этим данным, ионный обмен рассматривается как явление, происходящее между ковалентносвязан-ным водородом и гидратированным катионом в межплоскостной жидкости, причем сродство обратно пропорционально степени гидратации. Во время о бмена поляризованные гидратные оболочки перемещаются с занятого ими места, а выделяющиеся ионы водорода гидратируются. Общее изменение энтропии складывается из изменения энтропии за счет замещения одного катиона другим и разности энтропии гидратированных форм двух ионов. [28]
Изменение энтропии А5 не коррелируется с величинами гидрати-рованных ионных радиусов, однако оно линейно растет с увеличением радиуса иона как такового. Согласно этим данным, ионный обмен рассматривается как явление, происходящее между ковалентносвязан-ным водородом и гидратированным катионом в межплоскостной жидкости, причем сродство обратно пропорционально степени гидратации. Во время обмена поляризованные гидратные оболочки перемещаются с занятого ими места, а выделяющиеся ионы водорода гидратируются. Общее изменение энтропии складывается из изменения энтропии за счет замещения одного катиона другим и разности энтропии гидратированных форм двух ионов. [29]
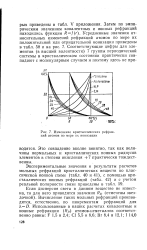 |
Изменение кристаллических рефракций атомов по мере их ионизации. [30] |
Страницы: 1 2 3 4