Величина - редокс-потенциал
Cтраница 2
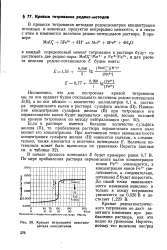 |
Кривая титрования восстано - ВИДНО из Уравнения Нернста, вителя окислителем. потому что величина окс / ред. [16] |
В процессе титрования методами редоксиометрии концентрации исходных и конечных продуктов непрерывно меняются, а в связи с этим и изменяется величина редокс-потенциалов раствора. [17]
Величина А / 70 равна сумме ( & F) 0 и ( А / 70), каждая из которых для одной и той же реакции зависит от величины редокс-потенциала комплексного иона - катализатора. [18]
 |
Величины нормальных редокс потенциалов Е некоторых хинонов в воде при 25 С. [19] |
Из данных, представленных в таблице 23 - 2, следует, что 1 2-хиноны более сильные окислители, чем 1 4-хиноны, а бензохиноны превосходят по окислительной способности хиноны нафталинового ряда, которые в свою очередь превосходят антрахиноны и фенантренхиноны. Электроноакцепторные группы усиливают окислительные свойства хинонов. Отметим попутно, что величины редокс-потенциалов коррелируют с энергией НСМО хинона. [20]
Если в раствор, содержащий окисленную и восстановленную формы одного и того же вещества, например Fe3 и Fe2, опустить платиновый электрод, то он приобретает определенный редокс-потенциал. Возникновение редокс-потенциала у индифферентного платинового электрода связано со способностью ионов Fe3 и Fe2 присоединять или отдавать электроны, находящиеся на платине - передатчике электронов. Происходит обмен электронами между инертным электродом и ионами. Если, например, окисленная форма Fe3 получает от платинового электрода электроны, восстанавливаясь до ионов Fe2, то электрод заряжается положительно, а раствор - отрицательно за счет избыточной концентрации анионов, например С1 -, если в растворе соль FeCls. Присоединение электрона ионом Fe3 становится постепенно более затруднительным и, наконец, устанавливается равновесие между положительно заряженным электродом и слоем анионов, определяющее величину редокс-потенциала. [21]
Страницы: 1 2