Величина - сила - межмолекулярное взаимодействие
Cтраница 1
Величины сил межмолекулярного взаимодействия и размеры молекул в жидкостях таковы, что эти перегруппировки при нормальной температуре протекают очень быстро, продолжаясь ничтожные доли секунды. [1]
Величина сил межмолекулярного взаимодействия должна быть достаточной для предотвращения взаимного перемещения макромолекул в сформованном волокне. Если величина межмолекулярных сил мала, то в результате взаимного перемещения макромолекул волокно будет подвергаться необратимым пластическим деформациям или обладать каучукоподобной эластичностью. [2]
Величина сил межмолекулярного взаимодействия должна быть достаточной для предотвращения взаимного перемещения макромолекул в сформованном волокне. Если величина межмолекулярных сил мала, то в результате взаимного перемещения макромолекул волокно будет подвергаться необратимым пластическим деформациям или обладать каучукоподобной эластичностью. [3]
Величина сил межмолекулярного взаимодействия должна быть достаточной, чтобы препятствовать взаимному передвижению макромолекул в сформованном волокне. [4]
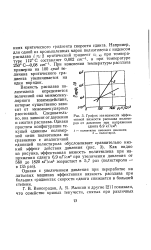 |
График зависимости эффективной вязкости расплава полимеров от давления при напряжении сдвига 6 9 кГ / слР. [5] |
Вязкость расплава полиэтилена определяется величиной сил межмолекулярного взаимодействия, которые существенно зависят от межмолекулярных расстояний. Следовательно, она зависит от давления и сжатия расплава. [6]
Химическое строение звеньев макромолекулярных цепей влияет на величину сил межмолекулярного взаимодействия. Полимеры, принадлежащие к группе алифатических углеводородов, не имеют полярных групп, поэтому в них связь между отдельными макромолекулами является только результатом действия дисперсионных сил. Дисперсионные силы межмолекулярного притяжения возникают вследствие поляризации молекул под влиянием непрерывного изменения взаимного положения электронов и ядер в каждом атоме, входящем в состав макромолекулы. Величина дисперсионных сил сравнительно мало зависит от температуры, но резко возрастает с уменьшением расстояния между макромолекулами. Силу межмолекулярного взаимодействия характеризуют величиной энергии когезии. Энергией к о-г е з и и называют энергию, которую необходимо затратить для удаления молекулы из твердого или жидкого тела. Величина энергии когезии приблизительно равна теплоте испарения при постоянном объеме. [7]
Недостатками полиорганосилоксанов являются невысокие адгезия и когезия, определяемые малой величиной сил межмолекулярного взаимодействия. Для повышения адгезии рекомендуется вводить в кремнийорганические мономеры полярные группы, а также модифицировать полиорганосилоксаны другими олигоме-рами и полимерами, например фенолоформальдегидными и фено-ло-анилиноформальдегидными смолами, акриловыми полимерами. [8]
Величина Тт определяется средней степенью полимеризации вещества, его полидисперсностью и величинами сил межмолекулярного взаимодействия. Для линейных полимеров одного и того же полимерно-гомологического ряда интервал температуры стеклования с повышением молекулярного веса нарастает в достаточно строгой пропорциональности, достигает максимума, характерного для данного соединения, после чего закономерная зависимость этих двух величин нарушается. Это явление положено в основу процесса пластификации смол, целью которого является увеличение температурного интервала проявления эластических деформаций. [9]
Недостатками всех кремнийорганических соединений являются невысокая адгезия и когезия, определяемые малой величиной сил межмолекулярного взаимодействия. Для устранения этих недостатков предложены различные методы. Так, рекомендуется вводить в кремнийорганические мономеры полярные группы, повышающие силы межмолекулярного воздействия, а также модифицировать кремнийорганические смолы соответствующими органическими соединениями. Присоединение к кремнийорганическим соединениям алкидных и эпоксидных групп повышает адгезионные свойства силиконов. [10]
Недостатками всех кремнийорганических соединений являются невысокие адгезия и когезия, определяемые малой величиной сил межмолекулярного взаимодействия. Для устранения этих недостатков предложены различные методы. Так, рекомендуется вводить в Кремнийорганические мономеры полярные1 группы, повышающие силы межмолекулярного воздействия, а также модифицировать Кремнийорганические смолы соответствующими органическими соединениями. Присоединение к кремнийорганическим соединениям алкидных и эпоксидных групп повышает адгезионные свойства силиконов. [11]
Силы, действующие между молекулами, также имеют электрическую природу, но порядок величины сил межмолекулярного взаимодействия значительно ниже сил, определяемых химическими связями. [12]
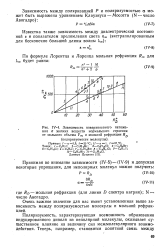 |
Зависимость поверхностного натяжения а жидких веществ нормального строения от мольного объема Vm и мольной рефракции RD. [13] |
Поляризуемость, характеризующая возможность образования индуцированного диполя из неполярной молекулы, оказывает существенное влияние на величину сил межмолекулярного взаимодействия. [14]
Влияние фазового состояния на процессы радиолиза проявляется, по-видимому, как следствие изменения упаковки молекул и величины сил межмолекулярных взаимодействий. Окрашивание аморфных веществ при облучении и образование в них радикалов, соответствующих вступлению в реакцию полярных групп молекул, делает очень вероятным предположение о гетеролитическом характере процессов радиолиза в этих веществах. Очевидно, эффективность гетеролитичееких реакций будет определяться концентрацией и природой дефектов структуры, способных локализовать заряды и увеличивать в результате этого время жизни ионов, образующихся при радиолизе. Как уже отмечалось, облученные образцы СзН8Оз Н2О имеют другую окраску, чем безводный глицерин, что может служить указанием на изменение центра локализации заряда. При небольших количествах воды в смеси изменение природы дефектов и, возможно, их концентрации приводит к увеличению эффективности гетеролитичееких реакций и, как следствие этого, к большим выходам радикалов. Значительное уменьшение выхода при изменении состава смеси от 1: 3 до 1: 6 связано, по-видимому, с тем, что структура замороженного раствора становится подобной структуре чистой воды, в которой, как известно, заряды не стабилизируются. [15]
Страницы: 1 2