Величина - смещение - полоса - поглощение
Cтраница 1
Величина смещения полос поглощения при переходе от газа к жидкости весьма непостоянна. Валентные колебания С - Н в ацетилене довольно чувствительны к физическому состоянию, вероятно, из-за ассоциации в растворах через мостиковые водородные связи. Для симметричных пятиатомных молекул теоретическое толкование проблемы было дано Хейкленом [116], который нашел, что длина связи увеличивается при переходе от пара к жидкости. [1]
Величины смещения полос поглощения других групп молекул ( например, валентных колебаний групп СН) при адсорбции менее значительны. Однако если колебания включают связи или звенья с сильно поляризующимися электронными орбитами ( я-электроны и свободные электронные пары), может происходить значительное изменение их интенсивности в результате нарушения симметрии распределения электронной плотности. При этом изменение спектра адсорбированных молекул может значительно превосходить по характеру и величине спектральные изменения в конденсированных средах и в инфракрасном спектре адсорбированных молекул начинают проявляться полосы поглощения, обычно слабые или полностью отсутствующие в спектре молекул в свободном состоянии. Такой эффект указывает на понижение симметрии молекулы и на ее ориентацию по отношению к поверхности. [2]
Величины смещений полосы поглощения свободных гидро-ксильных групп поверхности аэросила при адсорбции HCN, ацетонитрила и акрилонитрила указывают на уменьшение энергии специфического взаимодействия при переходе от синильной кислоты к ацетонитрилу и акрилонитрилу. [3]
Наблюдаемая большая разница в величинах смещения полосы поглощения валентных колебаний связей О - Н хлорной кислоты при добавлении к ней одного и того же количества Н3РО4 ( Av 340 слг1) или H2SC4 ( д 70 слг1) свидетельствует о значительно более сильных основных свойствах безводной ортофосфорной кисл. [4]
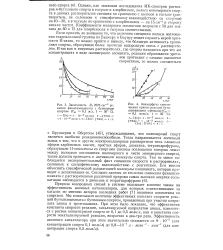
На этом рисунке приведены зависимости величин смещения полосы поглощения свободных гидроксильных групп аэросила, откачанного при 400 С, при адсорбции бензола и его алкилзамещенных от величины равновесного давления пара в кювете. Для всех адсорбирующихся веществ наблюдается возрастание величины AVOH с ростом заполнения поверхности до заполнений, соответствующих давлениям пара, при которых по адсорбционным данным заполняется монослой. С последующим увеличением давления наблюдается лишь очень медленное изменение положения полосы возмущенных при адсорбции гидроксильных групп. [5]
 |
Зависимость Dt 2270 см-1 реакции фенилизоциаиата с бутиловым спиртом ( С 0 1 м / л, t 50 С.| Анаморфозы кинетических кривых реакций бути-лизоцианата с фенолом ( См 0 1 моль / л, t 50 С. [6] |
Если принять во внимание то, что величина смещения полосы поглощения гидроксильной группы по Бэджеру и Бауэру может служить мерой прочности Н - связи, то можно прийти к выводу, что большую активность проявляют спирты, образующие более прочную водородную связь с растворителем. [7]
Галкиным, Киселевым, Лыги-ным ( 1964) исследована зависимость между величиной смещения Av полосы поглощения гид-роксильных групп и энергией взаимодействия адсорбированных молекул бензола и его алифатических производных с гидрокснль-ными группами кремнезема. [9]
В работах [ 13а, 44 - 47 ] сделана попытка сопостаЕйть величины смещения полосы поглощения поверхностных гидроксильных групп с величинами вкладов энергии специфического взаимодействия с этими группами в теплоту адсорбции. Эти величины являются независимо определяемыми энергетическими характеристиками адсорбционного взаимодействия. В противоположность значениям величин смещений полос поглощения свободных гидроксильных групп при адсорбции, AVOH - величины дифференциальных теплот адсорбции Q характеризуют сумму вкладов неспецифического и специфического взаимодействия с остовом кремнезема и поверхностными гидроксильными группами. Поэтому для всех молекул величины Q более чувствительны к геометрической и химической неоднородности поверхности. Поэтому для установления связи величин AVQH с тешютами адсорбции Q весьма важно, во-первых, выделение из общей теплоты адсорбции вклада, вносимого специфическим взаимодействием молекул с гидроксильными группами, и, во-вторых, выбор соответствующих заполнений поверхности 9, при которых изменение обеих величин определялось бы в основном одинаковыми факторами. Поэтому следует выбрать такие величины Э, при которых влияние неоднородности поверхности уже ослаблено, а влияние взаимодействия адсорбат - адсорбат еще не велико. [10]
Основность окиси этилена, однако, несколько меньше, чем простых эфиров и других циклических окисей ( окиси триметилена, диоксана); это следует из величины смещения полосы поглощения для связи О-D в инфракрасных спектрах растворов окисей вСН3ОО ( стр. Причина меньшей основности окиси этилена не выяснена. [11]
Было показано, что основность аминов можно оценить и путем сопоставления величин смещения максимума полосы поглощения в ИК-спектре, характерного для OD-связи, при растворении различных аминов в CH3OD, так как между величиной смещения полосы поглощения и основностью амина имеется прямая зависимость. [12]
Если на поверхности адсорбента имеются гидроксильные группы, то возможно возникновение водородной связи с участием атома серы. Сопоставление [223] теплот адсорбции, а также величин смещения полос поглощения валентных колебаний свободных ОН-групп S1O2 при адсорбции тиофенов и других соединений серы показывает, что эти величины коррелируют с донорной способностью атома серы в молекуле. [13]
Изменение положения полос поглощения колебаний в молекуле под действием водородных связей исследовано к настоящему времени весьма подробно. Для случая растворов уже накоплен большой материал по установлению зависимостей величин смещений полос поглощения и изменений их интенсивности от строения и свойств взаимодействующих групп. Точно так же среди различных применений спектроскопии к исследованию адсорбции наиболее изученными являются адсорбционные процессы, связанные с образованием водородной связи. [14]
Основными причинами трудностей в интерпретации электронных спектров являются их высокая чувствительность к различным особенностям внутри - и межмолекулярных взаимодействия и необходимость учета роли возбужденного состояния. Несмотря на то, что в настоящее время теоретические исследования дают возможность оценить направление, а в ряде случаев и величину смещения полос поглощения вследствие образования водородной связи [1, 14], а также произвести расчет универсального влияния растворителя на электронные спектры поглощения [15], непосредственное сопоставление с экспериментом затруднительно из-за указанных выше причин. Это усложняет использование проявлений водородной связи в электронных спектрах поглощения в качестве критерия с-е образования и разрушения, а также для оценки ее прочности. [15]
Страницы: 1 2
