Величина - теплота - растворение
Cтраница 1
Величина теплоты растворения обусловливается природой веществ, концентрацией полученного раствора и температурой. Величина теплоты растворения определенного количества вещества зависит от количества взятого растворителя. Различают теплоты растворения дифференциальную и интегральную. [1]
Величины теплоты растворения углеводородов С в водном растворе фурфурола, используемые в тепловых расчетах, даны в указанных работах Жордана и др. и Велти и др. Эти величины составляют 35 - 40 % от теплоты испарения углеводородов С. [2]
Знак величины теплоты растворения зависит от того, какая из двух слагаемых численно больше. [3]
Знак и величина теплоты растворения А / / в свою очередь определяются соотношением величин теплоты разрыва связей кристаллической решетки твердого вещества и теплоты гидратации. [4]
Было замечено, что величины теплот растворения в аммиаке больше, чем в воде, и при 25 С больше, чем при - 33 С. [5]
Авторы считают, что величина теплоты растворения хлорангидрида в том или ином растворителе может дать качественный ответ о возможности побочных реакций при поликонденсации. Растворители первой группы с отрицательной теплотой растворения авторы считают химически инертными по отношению к хлорангидриду изофталевой кислоты. Вторая группа растворителей имеет положительную теплоту растворения. Растворители второй группы вступают в химическую реакцию с хлорангидридом изофталевой кислоты. Теплота растворения хлорангидрида изофталевой кислоты в диметилформамиде равна 48 9 ккал / молъ. [6]
Вопрос о положительном или отрицательном значении величин теплот растворения постоянных газов и, в частности, кислорода в каучуках долгое время не был решен однозначно. В литературе имеются данные15, что растворимость кислорода в каучуке с увеличением температуры уменьшается; аналогичные наблюдения16 были сделаны относительно изменения растворимости водорода и азота в ряде эластомеров. [7]
На ряде веществ экспериментально установлен параллелизм между величиной теплоты растворения и кристаллическим состоянием вещества. [8]
Для одной неподвижной фазы влияние дипольного момента компонента на величину теплоты растворения мало заметно. Облако л-электронов фуранового цикла не позволяет осуществлять свободного вращения атомов углерода и легко поляризуется. На примере хроматографического поведения тетрагидрофурилового и фурилового спиртов показано участие л-электронов двойных связей фуранового цикла. Наличие дипольного момента по двойной связи и хорошая поляризуемость позволяют ненасыщенным фура-новым соединениям образовывать более сильную связь с полярными соединениями по сравнению с насыщенными гомологами. [9]
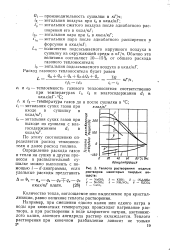 |
Теплота растворения водных растворов некоторых твердых веществ. [10] |
Количество тепла, поглощаемое или выделяемое при кристаллизации, равно величине теплоты растворения. [11]
Вопрос сводился к тому, являются ли значительные расхождения в величинах теплот растворения хлорида калия, накопленных к тому времени, следствием еще не обнаруженного полиморфизма последнего или существенна недостаточная чистота применяемых препаратов. Первую точку зрения, как известно, долго защищал Коген [ 48J, развивавший взгляд на полиморфизм как на универсальное свойство кристаллов, опираясь на обнаруженные еще Бертло и Илозвей [49] явления изменений теплот растворения некоторых солей во времени. [12]
Вопрос сводился к тому, являются ли значительные расхождения в величинах теплот растворения хлорида калия, накопленных к тому времени, следствием еще не обнаруженного полиморфизма последнего или существенна недостаточная чистота применяемых препаратов. Первую точку зрения, как известно, долго защищал Коген [48], развивавший взгляд на полиморфизм как на универсальное свойство кристаллов, опираясь на обнаруженные еще Бертло и Илозвей [49] явления изменений теплот растворения некоторых солен во времени. [13]
Следует установить, к каким именно растворам относятся данные, и вычислить для них величины теплот растворения на основе циклов Габера - Борна. [14]
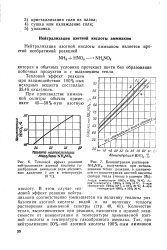 |
Тепловой эффект реакции.| Концентрация растворов. [15] |
Страницы: 1 2 3