Величина - теплота - смешение
Cтраница 1
Величины теплот смешения могут иметь значения от нескольких сот до единиц и даже десятых долей кал / моль. Весьма малые значения АЯ наблюдаются при исследовании разбавленных растворов. В том случае, когда зависимость АЯ от концентрации имеет 5-образную форму, малые значения АЯ будут наблюдаться и для ередней области концентраций. [1]
Величины теплот смешения в растворах высокомолекулярных веществ во многих случаях невелики. Это и понятно, так как часто молекулы растворителя близки по размерам и молекулярной природе к звеньям цепей полимеров, поэтому характер и величина взаимодействия между однородными и разнородными молекулами раствора одного и того же порядка. Теплота смешения действительно практически равна нулю в некоторых растворах, например Б растворах полиизобутилена ( М2 320000 и 90000) в изооктане и гуттаперчи в толуоле. [2]
Величины теплот смешения в растворах высокомолекулярных веществ во многих случаях невелики. Это и понятно, так как часто молекулы растворителя близки по размерам и молекулярной природе к звеньям цепей полимеров, поэтому характер и величина взаимодействия между однородными и разнородными молекулами раствора одного и того же порядка. Теплота смешения действительно практически равна нулю в некоторых растворах, например в растворах полиизобутилена ( Af2320000 и 90000) в изооктане и гуттаперчи в толуоле. [3]
Величины теплот смешения в растворах высокомолекулярных веществ во многих случаях невелики. Это и понятно, так как часто молекулы растворителя близки по размерам и молекулярной природе к звеньям цепей полимеров, поэтому характер и величина взаимодействия между однородными и разнородными молекулами раствора одного и того же порядка. Теплота смешения действительно практически равна нулю в некоторых растворах, например в растворах полиизобутилена ( / И8320 000 и 90 000) в изооктане и гуттаперчи в толуоле. [4]
Величины теплот смешения азеотропных компонентов играют важную роль во многих термодинамических расчетах и в теории образования азеотропов. Несмотря на это, и в настоящее время еще многие числовые данные о теплотах смешения отсутствуют. [5]
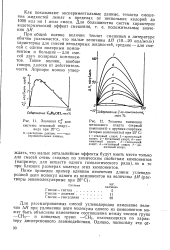 |
Теплоты смешения метилового спирта ( первый компонент с другими спиртами ( вторые компоненты при 25 С. [6] |
При общей оценке величин теплот смешения в литературе обычно указывается, что малые величины ДЯ ( 10 - 20 кал / моль) характерны для смесей неполярных жидкостей, средние - для смесей с одним полярным компонентом и большие - для смесей двух полярных компонентов. Такие оценки, вообще говоря, далеки от действительности. [7]
О комплексообразовании можно судить по величинам теплот смешения, которые могут быть определены с высокой точностью калориметрическим методом или рассчитаны по уравнению 30 на основе данных о равновесии между жидкостью и паром при различных температурах. В соответствии с термодинамической системой знаков эффект эндотермического процесса считается положительным, экзотермического - отрицательным. [8]
Возможно, что это обусловлено удачным подбором величин теплот смешения, отличия которых от действительно наблюдаемых компенсируют неточный расчет энтропии смешения. Кроме того, как показал В. А. Кожеуров [1], формулы, полученные без учета ближнего порядка, оказываются лучшим приближением к действительности в тех случаях, где существенную роль играет взаимодействие не только соседних, но и более удаленных частиц. Последнее обстоятельство, характерное для гетерополярйой связи, подтверждает тем самым ее доминирующую роль в шлаках. [9]
 |
Зависимость lg р от содержания воды в растворителе. 0 5 10 15 20. [10] |
О комплексообразо-вании ( или о сольватации) в растворе можно судить по величинам теплот смешения ( энтальпий смешения), которые легко определяют калориметрически или рассчитывают с помощью соответствующих термодинамических функций, а также волюметрически: в случае образования комплексов в растворе при смешении с растворителем происходит уменьшение общего объема. Оно тем больше, чем стабильнее комплекс, однако при этом может проявляться влияние структурных и других факторов. [11]
Рассмотрение имеющихся данных показывает, что при измерении тепловых эффектов смешения двух жидкостей с небольшим молекулярным весом ( С 100) наблюдается следующая приближенная зависимость между величиной теплоты смешения и изменением температуры калориметрической системы: при теплоте смешения ЛЯ R 100 кал / моль температура изменяется на несколько десятых градуса, при АЯ IQ кал / моль - на несколько сотых градуса, при ЛЯ - 1 кал / моль - на несколько тысячных градуса. Таким образом, для обеспечения точности измерения AT не менее 0 1 % необходимо измерять температуру в первом случае с точностью до 10 - град, во втором - до 10 - 5 град, в третьем - до 10 - 6 град. [12]
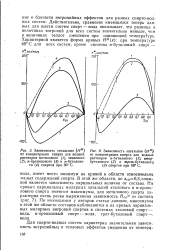 |
Зависимость энтальпии ( Н от концентрации спирта для водных растворов н-бутилового ( /, втор-бутилового ( 2 и / п /. е / и-бутиловогз ( 3 спиртов при 60 С. [13] |
Действительно, сравнение имеющихся теперь данных для шести систем спирт - вода показывает, что разница в величинах энтропии для всех систем значительно меньше, чем в величинах теплот смешения при одинаковой температуре. [14]
В работе Абе и Фуджита [18] отрицательный и нулевой температурный коэффициент невозмущенных размеров полистирола был получен по измерению характеристических вяз-костей в 6-смесях, причем зависимость KQ от температуры представляет линейную функцию, наклон которой определяется величиной теплоты смешения полимера с растворителем. [15]
Страницы: 1 2