Величина - число - перенос
Cтраница 1
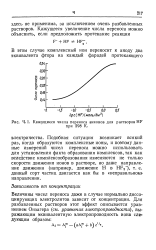 |
Кажущиеся числа переноса анионов для растворов HF. [1] |
Величины чисел переноса даже в случае нормально диссоциирующих электролитов зависят от концентрации. [2]
Величины чисел переноса тока, к экспериментальному определению и интерпретации которых обычно прибегают при исследовании механизмов электролитической диссоциации и переноса тока в разбавленных растворах, для исследования концентрированных растворов, вообще, и двойных жидких систем, в особенности, неприменимы. Прежде всего, с повышением концентрации становится неопределенным само понятие число переноса, так как в неводных растворах ( а в большинстве случаев двойные жидкие системы относятся к неводным растворам) диссоциация электролитов протекает не полностью. Вот почему было предложено при исследовании концентрированных растворов характеризовать степень участия различных частиц в переносе тока величиной, названной доля переноса тока, которая представляет собою количество грамм-эквивалентов данного компонента, переносимого через электролит одним фарадеем тока. [3]
Величины чисел переноса данного сорта ионов tj, как уже отмечалось, могут быть сделаны равными нулю; кроме того, миграция вообще отсутствует в случае незаряженных частиц. Величину коэффициента диффузии можно либо рассчитать, либо заимствовать из экспериментальных данных; определение величины начальной концентрации с также не представляет затруднений. Наименее определенной величиной является толщина диффузионного слоя, которая не может быть рассчитана в рамках теории Нернста - Брукнера. Ее определяют экспериментально, чаще всего из измерений предельной плотности тока. Опытные данные показывают, что б весьма мало зависит от состава раствора, но заметно меняется при изменении режима движения электролита. [4]
Следовательно, величина чисел переноса может быть определена по изменению концентрации электролита у электродон ли, что то жэ, по убыли веса вещества у анода и катода. [5]
В табл. 7.4 приведены величины чисел переноса катионов в указанных расплавах, сообщенные различными исследователями. Из данных таблицы следует, что разные методы определения чисел переноса катионов лития, натрия и калия дают весьма близкие результаты. [6]
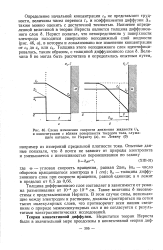 |
Схема изменения скорости движения жидкости. / т. [7] |
Определение начальной концентрации с0 не представляет трудности, величины чисел переноса t и коэффициентов диффузии А также можно оценить с достаточной точностью. [8]
Знак диффузионного потенциала, как это видно из уравнения ( 37), определяется соотношением величин чисел переноса катиона и аниона. [9]
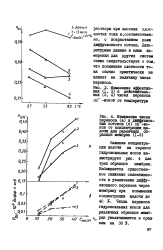 |
Изменение эффективи действительчисел переноса.| Изменение чисел переноса ( а и диффузионных потоков ( б он - ио-нов от концентрации щелочи StflS. pflf. JIM4HiJY 0 ( 5. [10] |
Литературные данные и наши измерения для других систем также свидетельствует о том, что повышение плотности тока обычно практически не влияет на величину чисел переноса. [11]
Концентрация электронных дефектов эквивалентна конщен трации междоузельных электронов. Величина чисел переноса ионов очень мала. [12]
Число переноса, являясь мерой относительной скорости движения иона, входящего в состав данного электролита, показывает вместе с тем, какая часть электричества переносится при прохождении тока через раствор данного электролита этим ионом. В этих приборах величину чисел переноса получают на основании определения изменения концентрации электролита в анодном и катодном слое при электролизе. Можно показать, что в том случае, если скорости движения ионов, входящих в данный электролит, одинаковы, то убыль вещества в анодном и катодном слое будет одинакова; если же равенства скоростей нет, то и убыль вешества у электродов будет различна. Последнее можно себе наглядно представить на следующих схемах. Пропустим через раствор такое количество электричества. [13]
При дальнейшем рассмотрении вопроса мы не будем вводить величину толщины диффузионного слоя, включив ее в константу скорости диффузии и считая условия конвекции постоянными. Количественно неопределимой оказывается также величина числа переноса иона в условиях изменяющейся концентрации диффузионного слоя. Получающиеся уравнения, поэтому, будут носить только качественный характер, и ценность их лишь в том, что они позволяют вскрыть общие закономерности электродного процесса, сопровождающегося чисто концентрационной поляризацией. [14]
Известно, что переносчиками тока в этом случае являются исключительно ионы [1, 3], вследствие чего применимы законы Фарадея. Нас будут интересовать такие типично электролитические свойства обсуждаемого класса жидкостей, как электропроводность, диффузия, процессы переноса ( например, величины чисел переноса анионов и катионов); кроме того, будет рассмотрено применение этих жидкостей в качестве электролитов в электролитических ячейках. [15]
Страницы: 1 2