Величина - электроотрицательность
Cтраница 1
 |
Величины электроотрицательных химических элементов. [1] |
Величина электроотрицательности для водорода приведена по Полингуэ. Величины в скобках оценены приблизительно. [2]
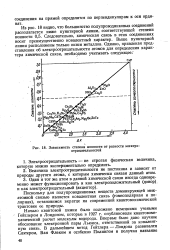 |
Зависимость степени ионности от разности электро-отрйцательностей. [3] |
Величина электроотрицательности не постоянна и зависит от природы другого атома, с которым химически связан данный атом. [4]
Сравнивая величины электроотрицательности у элементов различных групп и периодов, можно установить, какой из элементов обладает более металлическими свойствами. Элемент с меньшей электроотрицательностью проявляет более металлические свойства, чем элемент с большей электроотрицательностью. Характерно, что электроотрицательность как свойство элемента также является периодической функцией заряда ядра. [5]
Влияние величины электроотрицательности на свойства соединений неметаллов с ме - таллами уже было рассмотрено в гл. [6]
Разность величин электроотрицательности атомов ( см. табл. 5.18), образующих молекулу, определяет ионный или кова-лентный характер связи. [7]
По величине электроотрицательности углерод занимает промежуточное положение между типичными металлами и неметаллами, поэтому способность отдавать электроны у него почти такая же, как и присоединять электроны атомов других элементов. Следовательно, в химических соединениях углерод образует в основном ковалентные связи. [8]
По величине электроотрицательности кислород уступает толь ко фтору. Соединения кислорода с фтором являются уникальными, так как только в этих соединениях кислород имеет положительную степень окисления. [9]
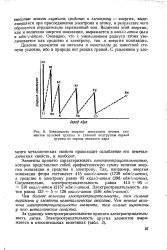 |
Зависимость энергии ионизации атомов элементов нулевой группы и главной подгруппы первой группы от заряда атомного ядра. [10] |
Чем больше величина электроотрицательности, тем сильнее выражены у элемента неметаллические свойства. Чем меньше величина электроотрицательности элемента, тем сильнее выражены у него металлические свойства. [11]
Чем выше величина электроотрицательности, тем больше способность атома присоединять к себе электроны, тем более неметаллический характер проявляет элемент. [12]
А - величина электроотрицательности гетероатома ( равная 3 9 - К) - 20 эрг - см для атома азота - N); if - его нормированная волновая функция. [13]
 |
Элекмроотрпцагелыюсть иекчпорых элементов но шкале. [14] |
Чем больше величина электроотрицательности данного атома, тем сильнее он притягивает электроны связи. В периодической системе элементов Д. И. Менделеева электроотрицательность растет снизу вверх и слева направо. [15]
Страницы: 1 2 3 4