Величина - эквивалентная электропроводность
Cтраница 2
С увеличением концентрации электролита наблюдается уменьшение величины эквивалентной электропроводности. [16]
Действия интерионных сил отражаются также на величине эквивалентной электропроводности, которая при разбавлении V, несмотря на полную диссоциацию, оказывается меньше, чем электропроводность при бесконечном разбавлении, так как в последнем случае частицы более удалены друг от друга, что и ослабляет их взаимодействие. [17]
 |
Схематическое изображение взаимосвязи удельной и эквивалентной электропроводности. [18] |
Поэтому при изучении растворов чаще пользуются величинами эквивалентной электропроводности. Эквивалентную электропроводность относят к 1 г-экв вещества и обозначают буквой Я. [19]
Этот метод приведен на рис. 20, причем использованы величины эквивалентной электропроводности, полученные Килпатриком и Луборским. Для пента-метилбензола, мезитилена и гексаметилбензола ожидаемая линейность приблизительно соблюдается. [20]
Кроме подвижности, в электрохимии вводится еще величина 1 - иР, представляющая собой величину эквивалентной электропроводности отдельного иона. Она равна произведению подвижности яонов на количество переносимого ионами электричества. [21]
В действительности Л возрастает по мере разбавления раствора, стремясь к максимальному значению при бесконечном разбавлении. Поэтому определяют величину эквивалентной электропроводности при бесконечном разбавлении Л, которая является характерным свойством каждого электролита. [22]
При разбавлении электролита, вследствие увеличения его степени диссоциации, эквивалентная электропроводность раствора непрерывно растет, пока не достигнет некоторой предельной величины. Это будет тогда, когда все молекулы распадутся на ионы, после чего дальнейшее разбавление раствора уже не будет изменять величину эквивалентной электропроводности. Последняя в этом случае называется эквивалентной электропроводностью при бесконечно большом разбавлении и обозначается через / то. [23]
Соотношения между степенью диссоциации и концентрацией электролита ( 171), а также между эквивалентной электропроводностью и концентрацией или разбавлением ( 172), ( 173) являются математическим выражением. Суть этого закона заключается в следующем: с разбавлением раствора ( с уменьшением концентрации) увеличивается степень диссоциации слабого электролита и величина эквивалентной электропроводности его, а константа диссоциации является постоянной величиной при данной температуре. [24]
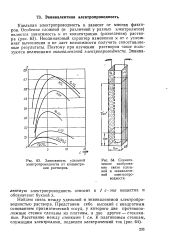 |
Зависимость удельной электропроводности от концентрации растворов.| Схематическое изображение связи удельной и эквивалентной электропроводности. [25] |
Удельная электропроводность х зависит от многих факторов. Неодинаковый характер изменения к от с усложняет вычисления и не дает возможности получить сопоставляемые результаты. Поэтому при изучении растворов чаще пользуются величинами эквивалентной электропроводности. [26]
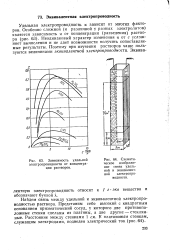 |
Зависимость удельной электропроводности от концентрации растворов.| Схематическое изображение связи удельной и эквивалентной электропроводности. [27] |
Удельная электропроводность к зависит от многих факторов. Неодинаковый характер изменения к от с усложняет вычисления и не дает возможности получить сопоставляемые результаты. Поэтому при изучении растворов чаще пользуются величинами эквивалентной электропроводности. [28]
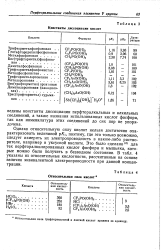 |
Относительная сила кислот. [29] |
Однако относительную силу кислот нельзя достаточно охарактеризовать величиной р / Сь поэтому, где это только возможно, следует измерить их электропроводность в каком-либо растворителе, например в уксусной кислоте. Это было сделано 101 для тех перфторалкилированных кислот фосфора и мышьяка, которые можно было получить в безводном состоянии. В табл. 4 указаны их относительные кислотности, рассчитанные на основе величин эквивалентной электропроводности при данной концентрации. [30]
Страницы: 1 2 3