Величина - энергия - ионизация
Cтраница 2
Электронофильность проявляется в величинах энергии ионизации, электронного сродства, электроотрицательности элементов, ре-доксо-потенциалах, однако ни одним из этих показателей однозначно не определяется. Электронофильность частиц ( атомов, ионов) играет основную роль в реакциях окисления - восстановления, определяя их направленность и интенсивность. Электронейтральные атомы металлов, как правило, проявляют меньшую Электронофильность, чем неметаллов, катионы более электронофильны, чем электронейтральные атомы - и тем сильнее, чем выше заряд и меньше радиус катиона. [16]
Заметим наконец, что величина энергии ионизации связана с энергетическим состоянием электрона: первый потенциал ионизации бора ниже, чем бериллия, так как удаляется 2р - электрон, более подвижный, чем 2-электрон бора. То же самое наблюдается в случае алюминия и магния. [17]
Обратим внимание на то, что величины энергии ионизации ( работа отрыва электрона от атомной структуры) хорошо иллюстрирует дискретность поля ядра. Здесь видно, что величина работы отрыва очередного электрона довольно круто повышается по ходу оголения ядра. Переход от одного энергетического уровня к другому, более высокому, на общей кривой проявляется изломами, что говорит о скачкообразном характере процесса постепенной ионизации как результат дискретности поля ядра. [18]
При образовании соединения из двух атомов величины энергии ионизации и их сродства к электрону, рассматриваемые изолированно друг от друга, не могут служить мерой для характеристики тенденции каждого из них к образованию положительного или отрицательного иона. [19]
Величина энергии сродства к электрону значительно меньше величины энергии ионизации тех же атомов. Обе эти величины изменяются в зависимости от изменения величины заряда ядра и размеров атома: с увеличением заряда ядра они должны увеличиваться, а с увеличением радиуса атома уменьшаться. В связи с этим в каждом периоде наблюдается увеличение энергии ионизации от щелочных металлов к инертным элементам. В вертикальных же группах дело обстоит сложнее: в главных подгруппах увеличение радиуса атомов сверху вниз перекрывает увеличение заряда ядер и потому энергия ионизации от верхних элементов к нижним уменьшается; в побочных же подгруппах этого перекрывания не наблюдается и потому энергия ионизации изменяется не столь явно. Что касается энергии сродства к электрону, то она вообще изменяется симбатно с изменением энергии ионизации, но, поскольку величины энергии сродства к электрону малы по сравнению с величинами энергии ионизации, изменения первых бессмысленно наблюдать у элементов, расположенных в левой и нижней частях периодической системы; кроме того, энергия сродства к электрону, увеличиваясь для элементов от четвертой до седьмой главных подгрупп, резко падает от седьмой к восьмой главной подгруппе. Изменение величины ионизационных потенциалов в зависимости от порядкового номера элемента графически показано на рис. 1.1. На рис. 1.2 приведена зависимость изменения радиусов атомов от порядкового номера. [20]
Мерой прочности связи электронов в атомах является величина энергии ионизации, или ионизационного потенциала ( гл. Очевидно, что восстановительная способность металлов связана с величиной энергии ионизации их атомов. Наименьшие значения ионизационного потенциала у щелочных металлов, которые и являются самыми энергичными восстановителями. [21]
Величина энергии сродства к электрону значительно меньше величины энергии ионизации тех же атомов. Обе эти величины изменяются в зависимости от изменения величины заряда ядра и размеров атома: с увеличением заряда ядра они должны увеличиваться, а с увеличением радиуса атома уменьшаться. В связи с этим в каждом периоде наблюдается увеличение энергии ионизации от щелочных металлов к инертным элементам. В вертикальных же группах дело обстоит сложнее: в главных подгруппах увеличение радиуса атомов сверху вниз перекрывает увеличение заряда ядер и потому энергия ионизации от верхних элементов к нижним уменьшается; в побочных же подгруппах этого перекрывания не наблюдается и потому энергия ионизации изменяется не столь явно. Что касается энергии сродства к электрону, то она вообще изменяется симбатно с изменением энергии ионизации, но, поскольку величины энергии сродства к электрону малы по сравнению с величинами энергии ионизации, изменения первых бессмысленно наблюдать у элементов, расположенных в левой и нижней частях периодической системы; кроме того, энергия сродства к электрону, увеличиваясь для элементов от четвертой до седьмой главных подгрупп, резко падает от седьмой к восьмой главной подгруппе. Изменение величины ионизационных потенциалов в зависимости от порядкового номера элемента графически показано на рис. 1.1. На рис. 1.2 приведена зависимость изменения радиусов атомов от порядкового номера. [22]
Из приведенных данных видно, что по величине энергии ионизации водород стоит значительно ближе к фтору, чем к литию, и никакие металлические свойства свободному атому водорода, следовательно, не присущи. Точно так же положительно заряженный ион водорода не имеет ничего общего со свойствами ионов щелочных металлов, поскольку является элементарной частицей - протоном. Вместе с тем в электрохимическом ряду напряжений водород ведет себя как металл. Это объясняется тем, что электрохимический ряд напряжений служит характеристикой атомов металлов в водных растворах ( см. гл. При ионизации атома водорода в присутствии воды образуется ион гидроксония Н3О, что сопровождается выделением энергии. Вследствие этого энергия ионизации атома водорода в водном растворе резко снижается и становится близкой к величине энергии ионизации атомов металлов. Заметим, что по некоторым физическим свойствам ион НзО в растворе ведет себя подобно катионам щелочных металлов. Однако эти особенности не относятся к атому или иону водорода и не дают оснований рассматривать его как металл. Сходство строения внешней электронной оболочки атома водорода с внешними электронными оболочками атомов щелочных металлов носит, следовательно, такой же формальный характер, как и однотипность строения внешних электронных оболочек атома гелия и атомов элементов II группы. [23]
Превращение атомов в положительно заряженные ионы определяются величиной энергии ионизации наружных электронов ( стр. Чем меньше энергия ионизации элемента, тем ярче выражены его восстановительные свойства. Энергия ионизации первого электрона, считая снаружи, является периодической функцией зарядов атомных ядер. Наименьшее значение энергии ионизации наблюдается у элементов, в атомах которых внешний энергетический уровень содержит только s - электроны и один или редко два р-электрона. По мере увеличения числа электронов в / - подуровне наружного энергетического уровня энергия ионизации резко возрастает. [24]
Обращает на себя внимание резкое различие в величинах энергии ионизации атомов сравниваемых элементов. [25]
У кислорода по сравнению с атомом азота падает величина энергии ионизации, что вызвано спариванием электронов. При этом каждый из трех 2р - электронов располагается на одной из трех2р - орбиталей. В атоме кислорода на этом втором уровне появляется шестой электрон, так как уже нет свободной 2р - орбитали, то этот электрон вынужден располагаться на одной из тех 2р - орбиталей, где уже есть электрон. Межэлектронное отталкивание резко возрастает и перекрывает эффект действия заряда ядра. Кислород ионизируется легче, чем азот. Этим, между прочим, объясняется содержание ионосферы Земли, где много озона и ионов кислорода. Атом О имеет электронную конфигурацию: Is22sz2px22pyl2pzl, в которой находятся два неспаренных электрона. [26]
Радиус катиона Li меньше радиуса катиона К и соотношение величин энергий ионизации и гидратации для лития оказывается таким, что у него в водном растворе отнять электрон легче, чем у атома калия. [27]
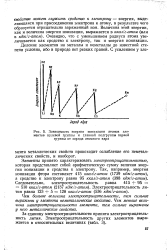 |
Зависимость энергии ионизации атомов элементов нулевой группы и главной подгруппы первой группы от заряда атомного ядра. [28] |
Элементы принято характеризовать электроотрицательностью, которая представляет собой арифметическую сумму величин энергии ионизации и сродства к электрону. [29]
При вычислениях часто делается предположение, что произведение 2nfivo равно величине энергии ионизации. Из сравнения значений 2nfiv0, найденных оптическим методом [48], и энергии ионизации / [50] видно ( табл. 2), что это предположение не всегда оправдывается. [30]
Страницы: 1 2 3 4