Величина - энергия - активация
Cтраница 1
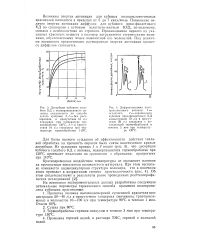
Величины энергии активации изменяются в различных опытах от 53 400 до 67 200 - кал и значения С от 29 до 33 в температурных пределах от 400 до 6009 С. Энергия активации уменьшается с повышением температурь кипения продукта. При одинаковом молекулярном весе ароматические продукты имеют более высокие значения энергии активации, чем парафинистые продукты. [1]
Величина энергии активации, необходимой для перемещения водорода в водородных связях рассматриваемого типа, ни разу не определялась экспериментально. Этот случай, однако, резко отличается от рассматриваемого, что будет подробнее обсуждено ниже ( см. стр. [2]
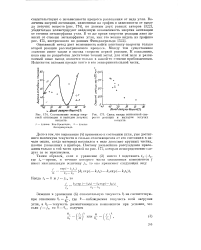 |
Соотношение между энергией активации и выходом летучих веществ.| Связь между константой скорости реакции и выходом летучих веществ. [3] |
Величины энергий активации, нанесенные на график в зависимости от выхода летучих веществ ( рис. 174), по данным двух разных авторов [322], убедительно иллюстрируют найденную независимость энергии активации от степени метаморфизма угля. [4]
Величина энергий активации для галоидных комплексов [ ( М - Галоид) ( MAlk) ], по всей вероятности, несколько ниже величины, приведенной для кисных центров, и может быть оценена примерно значением 10 ккал. Теплота образования комплекса [ AlCl3 - AlAlk3) составляет примерно 1 - 5 ккал, теплота адсорбции пропилена на поверхности TiCl3 может быть также близка к 4 - 5 ккал. Принимая Ер равной опять-таки 10 ккал н добавляя все составляющие, мы получим величину суммарной энергии активации 8 - 12 ккал, что согласуется с рассмотренными результатами. [5]
Величины энергии активации для кубовых полициклокетоновых красителей находятся в пределах от 5 до 7 ккал / моль. Повышение величин анергии активации диффузии для кубового ярко-фиолетового КД по сравнению с кубовым золотисто-желтым КХД, по-видимому, связано с особенностями их строения. Проникновение первого из указанных красящих веществ в полимер затрудняется стерическими помехами, обусловленными менее компактной его молекулой. Под влиянием введенного органического растворителя энергия активации процесса диффузии снижается. [7]
Величины энергий активации, полученные для процесса диффузии в объеме и по граничным поверхностям окислов в отдельности, яснее конкретизируют рассматриваемый диффузионный процесс. Однако ориентация только на величину энергии активации для представления о порядке величины коэффициента диффузии не может быть достаточной. [8]
Величина энергии активации может быть определена несколькими методами; во-первых, методом расчета данных зависимости константы скорости от температуры, полученных экспериментальным путем. [9]
Величина энергии активации зависит от работы образования дырки для иона, диффундирующего в зерне ионита, и от работы перемещения иона в сильном электростатическом поле внутри зерна ионита. В водном растворе работа не зависит от размера катиона и в процессе самодиффузии практически постоянна. Распределение ионов в электростатическом поле определяется диэлектрической постоянной среды, степенью ассоциации ионов и расстояниями между ними. Расстояние между двумя положениями равновесия должно сильно зависеть от заряда ионов, причем в большей степени для одновалентных ионов, чем для трехвалентных. При увеличении поперечных связей ионы подходят ближе друг к другу и расстояния между двумя положениями равновесия уменьшаются. [10]
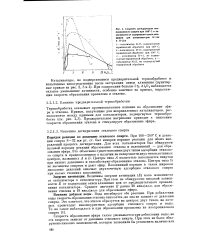 |
Скорость дегидратации изо-пропилового спирта при 100 С в зависимости от содержания окиси алюминия для катализаторов К-14 х и К-25 х. [11] |
Величины энергии активации ( Е) мала изменяются от катализатора к катализатору. При этом не обнаружено никакой зависимости Е от содержания окиси алюминия или от предварительного прокаливания катализатора. Среднее значение Е равно 28 ккал / моль для образования этилена и 18 ккал / молъ для образования эфира. [12]
Величина энергии активации зависит от энергетического состояния молекул, вступающих в химическую реакцию. Для реакций между валентно-насыщенными молекулами процесс активации очень часто заключается в коммулировании энергии на одной из связей молекулы, приводящем к разрыву связи и являющемся началом реакционного процесса. В этих случаях энергия активации близка к энергии разрыва связи и составляет несколько десятков килокалорий. [13]
 |
Изотермы термического окисления кремния в водяном паре при Ян О 1 атм. [14] |
Величина энергии активации заметно зависит от состояния исходной поверхности кремния и наличия на ней хемосорбированных примесей того или иного типа. По эффективной энергии активации можно условно сделать вывод о наиболее медленно протекающей ( контролирующей) стадии процесса. При этом интервал 40 - 120 кДж / моль ( 10 - 30 ккал / моль) характеризует преимущественно диффузионный контроль, интервал 280 - 400 кДж / моль ( 70 - 100 ккал / моль) определяет преобладание поверхностной реакции, а промежуточные значения энергии активации отвечают смешанному контролю. [15]
Страницы: 1 2 3 4 5