Величина - энергия - гиббс
Cтраница 2
Абсолютные значения энергии Гиббса системы определить невозможно, поскольку в энергию Гиббса входит величина энтальпии. Величину энергии Гиббса можно лишь выразить в виде разности энергий Гиббса двух различных состояний, одно из которых принято за стандартное. VIII приведены термодинамические величины для стандартного состояния каждого из элементов, входящих в органические соединения, а также данные для некоторых важных неорганических соединений. Аналогичные величины для стандартных состояний органических веществ представлены в виде таблиц в последующих главах. [16]
Если энергия Гиббса при данных Т и Р минимальна, что соответствует равновесному состоянию системы, то это положение может быть непосредственно применено к нахождению равновесного соства реакционной смеси без предшествующей спецификации каких-либо стехиометрических отношений. Единственная необходимая информация - это величины энергии Гиббса образования всех химических компонентов, которые могут присутствовать в системе в условиях равновесия, и характер изменения их фугитивностей или коэффициентов активности, если их нельзя принять равными единице. Этот метод отличается гибкостью по отношению к возможным компонентам, так как по завершении расчетов выясняется, что концентрации лишних компонентов пренебрежимо малы. [17]
ОЗ есть постоянная величина. В общем случае, чем более отрицательна величина энергии Гиббса образования оксида RxOy, тем меньше произведение активностей кислорода и раскислителя R и, следовательно, тем ниже концентрация остающегося в железе кислорода при данном расходе раскислителя. [18]
Расчет давления СО осуществляют по величине константы равновесия Кр, которую рассчитывают по величине энергии Гиббса. [19]
Для полного протекания реакции необходимо, чтобы равновесное давление СО было близко к 1 атм или превышало ее. Расчет давления СО осуществляют по величине константы равновесия КР, которую рассчитывают по величине энергии Гиббса. [20]
Так как фазовые равновесия определяются свойствами фаз при условиях их сосуществования, то в результате решения этих задач можно, вообще говоря, надеяться на получение термодинамических данных только вдоль границ равновесия фаз. Как уже говорилось, цель расчетов можно считать достигнутой, если в каждой точке кривой или поверхности равновесия фаз станут известны величины энергии Гиббса и всех ее первых частных производных по термодинамическим переменным, что эквивалентно в общем случае знанию на фазовой границе энтальпии, энтропии, объема и химических потенциалов всех компонентов фазы и, естественно, любых других функций, являющихся комбинацией вышеназванных. Это не исчерпывающая информация о термодинамике системы на фазовой границе, так как остаются неопределенными высшие производные термодинамического потенциала. Но такой информации достаточно, чтобы находить энергии Гиббса в области гомогенности фазы, непосредственно примыкающей к границе ее существования, и это максимум того, что можно извлечь из условий гетерогенного равновесия, не прибегая к вне-термодинамическому моделированию функциональных зависимостей свойств. [21]
Интересно рассмотреть связь коэффициентов диффузии с понятием подвижности, которое мы ввели при рассмотрении электропроводности. Подвижность - это скорость, которую приобретает частица при действии единичной силы. Если в двух точках раствора концентрация различна, то и величина парциальной молярной энергии Гиббса компонента Gm в этих точках будет разной. Следовательно, при переходе молекулы из одной точки в другую будет производиться работа, равная убыли энергии Гиббса: W-Gm, где индекс т указывает на то, что энергия Гиббса относится не к молю, а к молекуле. Но работа равна произведению силы на путь. [22]
С первого взгляда кажется весьма трудным определить экономическую ценность такой информации. Данные по равновесиям процессов, протекающих при переработке нефти, могут быть неоднократно использованы при решении конкретных технологических проблем. При этом следует отметить, что если для какого-либо соединения известна величина энергии Гиббса, то ее можно использовать в расчете равновесия любой другой реакции, для всех остальных участников которой имеются соответствующие величины энергии Гиббса. Именно поэтому многократное использование полученных данных в решении постоянно возникающих задач анализа термодинамического равновесия полностью оправдывает первоначальную затрату на получение исходной информации. [23]
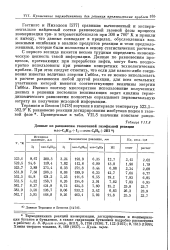 |
Данные по равновесию гомогенной газофазной реакции. [24] |
С первого взгляда кажется весьма трудным определить экономическую ценность такой информации. Данные по равновесиям процессов, протекающих при переработке нефти, могут быть неоднократно использованы при решении конкретных технологических проблем. При этом следует отметить, что если для какого-либо соединения известна величина энергии Гиббса, то ее можно использовать в расчете равновесия любой другой реакции, для всех остальных участников которой имеются соответствующие величины энергии Гиббса. Именно поэтому многократное использование полученных данных в решении постоянно возникающих задач анализа термодинамического равновесия полностью оправдывает первоначальную-затрату на получение исходной информации. [25]
Страницы: 1 2