Величина - энтальпии
Cтраница 1
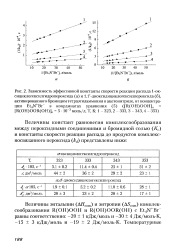
Величины энтальпии ( АЯсот) и энтропии ( А5сот) комплексообразования R ( OH) OOH и R ( OH) OOR ( OH) с Et4N Br равны соответственно: - 20 1 кДж / моль и - 30 4 Дж / моль - К, - 15 3 кДж / моль и - 19 2 Дж / моль - К. [2]
Величина энтальпии здесь выражена через параметры состояния и, следовательно, также представляет собой параметр состояния термодинамической системы. [3]
Величина энтальпии 1п 5ДЯ298 - 33 6ккал / град-моль [586] указывает на неустойчивость соединения, существующего в газовой фазе и при конденсации в твердом виде распадающегося на InS и металлический индий. [4]
Величины энтальпии ( АЯсот) и энтропии ( А5сот) комплексообразования R ( OH) OOH и R ( OH) OOR ( OH) с Et4N Br равны соответственно: - 20 1 кДж / моль и - 30 4 Дж / моль - К, - 15 3 кДж / моль и - 19 2 Дж / моль - К. [6]
Величины энтальпии согласуются с величинами парциальных изменений энтальпии поливинилхлорида и пластификатора. [7]
Величина энтальпии у идеального газа зависит только от температуры газа, а у реального, кроме того, и от давления. [8]
Величины энтальпии растворения С60 в насыщенные растворы в четы-реххлористом углероде и толуоле представлены в табл. 3.1. Значение теплоты растворимости С60 в насыщенный раствор в четыреххлористом углероде ниже ТМР превышает величину энтальпии плавления фуллерена С60 на 9 кДж / моль, что составляет 45 % отклонения растворов от идеального по эндотермическому типу. Вероятно, что насыщенные растворы С60 в четыреххлористом углероде при температурах ниже ТМР находятся в равновесии с твердым кристаллосоль-ватом. Тогда интегральная теплота растворимости в данном случае содержит эндотермический член, отвечающий теплоте плавления образующегося кри-сталлосольвата. Данный вывод согласуется с положениями термодинамической модели [3], где также допускается, что растворы С60 находятся в равновесии с твердым кристаллосольватом. [9]
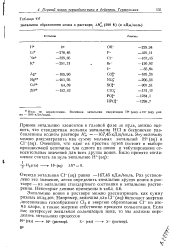 |
Энтальпии образования ионов в растворе, Л / / т ( 298 К ( в кДж / Чюль. [10] |
Величина энтальпии гидратации 11 ( газ) - - HT ( aq) равна - 1090 кДэк / моль. [11]
Величина энтальпии изомерных превращений определяется такими факторами, как изменение числа алкильных заместителей в цепи и их относительное расположение. Всякое появление ме-тильного ( алкильного) заместителя, как правило, сопровождается энергетическим выигрышем, достигающим в среднем величины 2000 - 2500 кал / моль. Однако каждый новый заместитель образует энергетически неблагоприятные скошенные взаимодействия как с основной цепью, так и с имеющимися заместителями. Поэтому существует определенное, оптимальное для данной длины цепи, количество заместителей и отсюда - оптимальные соотношения нормальных, монозамещенных, дизамещенных и триметилзамещенных углеводородов. [12]
Величина энтальпии твердых веществ повышается с продолжительностью нагрузки не монотонно ( например, при увеличении длительности размола), а проходит через максимум и минимум. Например, при длительном измельчении искажения решетки могут залечиваться. Таким образом, активности проходят через максимум, который следует принимать во внимание при химических превращениях. [13]
Величина энтальпии идеального газа зависит только от его температуры, а у реального, кроме того, - от давления. [14]
Величина энтальпии сгорания данного вещества, естественно, зависит как от состояния, в котором находятся участвующие в реакции вещества, так и от температуры, к которой относится процесс, и давления, при котором он протекает. [15]
Страницы: 1 2 3 4