Величина - энтальпии
Cтраница 3
Экспериментально установлено, что величина энтальпии среды в трубе экрана парогенератора сверхкритических параметров влияет на количество отложившихся окислов железа сильнее, чем тепловой поток. [31]
Отсюда следовало, что величина энтальпии циклизации для производных е-капролактама должна быть меньше, чем для незамещенного е-капролактама. Действительно, оцененные в этой работе значения ДЯ реакции полимеризации для производных е-капролактама оказались меньше, чем для незамещенного е-капролактама. Однако все найденные величины ДЯ оказались значительно больше по величине, чем определенные в других работах. [32]
Отклонения вычисленных таким образом величин энтальпии от величин, приведенных в таблицах [2], указаны на фиг. Эти отклонения значительно меньше допустимых отклонений международных эталонных таблиц и обычно имеют гот же порядок, что и в таблицах других авторов. [33]
Полученные авторами указанных работ величины энтальпии сублимации хорошо ( с отклонениями в пределах 1 - 2 ккал / моль) согласуются с результатами наших определений весовыми методами Кнудсена и Лэнг-мюра, а также, с данными микрокалориметрических измерений. Эти исследования позволяют подойти к решению вопросов механизма межмолекулярного взаимодействия азотистых оснований в молекулах нуклеиновых кислот. [34]
Достаточно просто, используя величину энтальпии испарения жидкой воды ( 10 4 ккал / модь при 25 С), оценить величины энтальпий образования перечисленных газогндра-тов из газообразных ионов и жидкой воды. Экспериментальные результаты Кебарле относятся к газогидратам, близким к состоянию насыщения: как было показано, каждая последующая молекула воды, присоединенная к газогидрату, приводит к оводнению последнего. В графе Ш табл. 1 приведены данные, характеризующие энергию взаимодействия иона с одной молекулой воды в газогидрате, близком к состоянию насыщения. Эти данные свидетельствуют о том, что связь ионов лития и натрия с молекулой воды сильнее, чем энергия водородной связи в жидкой воде ( - 5 5 ккал), а для ионов калия, рубидия и цезия наблюдается противоположная ситуация. [35]
При этом должны быть известны величины энтальпии и энтропии для начального и конечного состояний. [36]
Мак-Дональд [968] нашел, что величина энтальпии испарения 1 2-дихлорэтана при 298 К равна 8470 20 кал / моль. Это значение хорошо согласуется с приведенной выше величиной энтальпии образования, определенной Зинке и Сталлом методом калориметрии сгорания. [37]
Воспользуемся тем, что известна величина энтальпии системы жидкость - пар, определены значения массовых долей ха и х -, приравнены скорости изменения температуры металла и более нагретой фазы. [38]
Мак-Дональд [968] нашел, что величина энтальпии испарения 1 2-дихлорэтана при 298 К равна 8470 20 кал / моль. [39]
С использование уравнения Вант-Гоффа рассчитаны величины энтальпии межфазного распределения. Оказалось, что если для ( 1) и ( 2) энтальпии экстракции достаточно близки и составляют соответственно 2 6 и 3 0 кДж / моль, то для ( 3) эта величина достигает 10 6 кДж / моль. Последнее, по-видимому, может быть связано с возможностью бидентатного связывания двух гидроксильных групп молекулы пирокатехина при образовании экстрагируемого комплекса с МТБЭ. [40]
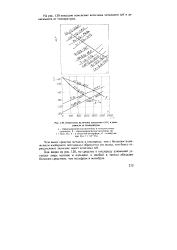 |
Изменение величины энтальпии ( Л / / в зависимости от температуры. [41] |
На рис. 130 показано изменение величины энтальпии Д / / в зависимости от температуры. [42]
Прежде чем приступить к расчету величины энтальпии водяного пара по данным опыта, следует для каждого режима усреднить записанные значения измеряемых а опыте величин и в расчете использовать именно эти усредненные значения. [43]
Прежде чем приступить к расчету величины энтальпии водяного пара по данным опыта, следует для каждого режима усреднить записанные значения измеряемых в опыте величин и в расчете использовать именно эти усредненные значения. [44]
Для создания надежной расчетной схемы имеющихся величин энтальпии сублимации алифатических полинитросоединений недостаточно. [45]
Страницы: 1 2 3 4