Величина - индуктивный эффект
Cтраница 1
Величина индуктивного эффекта в ряде случаев недостаточна для того, чтобы объяснить стабильность полиалкилзамещенных карбокатио-нов, например mpem - бутил-катиона. [1]
Величина индуктивного эффекта растет с величиной заряда на заместителе. [2]
Знак и величина индуктивного эффекта определяются различиями в электроотрицательности между рассматриваемым атомом углерода и группой, его вызывающей. [3]
Поскольку от величины индуктивного эффекта зависит и способность молекул к образованию координационной связи с молекулами воды, растворимость хлорбензола должна быть больше, чем растворимость иодбензола, что и наблюдается в действительности. В случае нитробензола оба эффекта нитрогруппм - индуктивный и сопряжения - действуют в одном направлении, понижая электронную плотность бензольного кольца и придавая ему благодаря этому избыточный эффективный положительный заряд. Последний в ядре нитробензола превышает заряд в ядре хлорбензола, в молекуле которого индуктивный эффект и эффект сопряжения действуют в противоположных направлениях. [4]
Главную роль в величине индуктивного эффекта играет заряд на центральном атоме группы, т.е. на атоме, непосредственно связанном с углеродной цепочкой, по которой эффект передается к реакционному центру. К группам с огромным отрицательным индуктивным эффектом относятся диазо-группа ( - N N) и фенилгалогеноиневые группы ( - Cl Ph, - Br Ph, - I Ph); меньшим, но все же достаточно большим индуктивным эффектом обладают триметиламмонийная группа ( - К Мез) и нитрогруппа ( - N ( O) O -) с положительным зарядом на атоме азота. Отрицательно заряженные группы ( - О, - СОО, ЕГ ( ОН) з) проявляют ( /) - эффект, т.е. отталкивают электроны. [5]
Хотя разница в величине индуктивного эффекта для различных алкильных групп невелика, этого вполне достаточно, чтобы дипольные моменты алкилгалогеиндов не подчинялись правилу векторных сумм, о чем говорилось в начале этого раздела. [6]
При оценке реакционной способности заместителей в полимерной матрице нонита необходимо учитывать не только величину индуктивного эффекта и электронной плотности, но и сте-рические факторы, которые приведут к преимущественному замещению групп в пара-положении. [7]
Легкость металлирования в о-положении к галоиду в ароматическом соединении, как известно, изменяется в соответствии с величиной индуктивного эффекта заместителя в порядке F C1 Br J [82], хотя в ряду тиофена такой сравнительный анализ не проводился. Литирование галоидтиофенов проходит легко, если не осложняется другими реакциями, главная из которых - литий-галоидный обмен, особенно характерный для Вг - и J-за-мещенных тиофена, но иногда наблюдающийся и в случае хлор-тиофенов. [8]
Из своих расчетов Фукуи и соавторы сделали выводы о том, что бензольное кольцо притягивает с-электроны, что величина индуктивного эффекта может быть охарактеризована значениями суммарных зарядов атомов, что электронная плотность заместителя тем выше, чем более он электроотрицателен. Авторы полагают также, что согласно их расчетам, распределение с-электронов не должно играть важной ориентирующей роли в реакциях замещения, свойственных ароматическим соединениям. [9]
Можно сделать вывод, что даже в тех случаях, когда скорость пара-замещения соответствует индуктивному ряду заместителей, проявляется также и эффект гиперконъюгации, по величине сравнимый, но однако не превышающий величину индуктивного эффекта. [10]
По результатам расчетов сг-электронных зарядов атомов и связей в ненасыщенных соединениях Фукуи и соавторы ( 1962) сделали вывод, что бензольное кольцо притягивает а-электроны ( кроме, может быть, в некоторых случаях атома углерода, непосредственно связанного с заместителем), что величина индуктивного эффекта может быть охарактеризована значениями а-эдектронных зарядов атомов, но что в общем а-электронное распределение не должно играть ориентирующей роли в реакциях замещения, свойственных ароматическим соединениям. [11]
По результатам расчетов о-электронных зарядов атомов и связей в ненасыщенных соединениях Фукуи и соавторы ( 1962) сделали вывод, что бензольное кольцо притягивает а-электроны ( кроме, может быть, в некоторых случаях атома углерода, непосредственно связанного с заместителем), что величина индуктивного эффекта может быть охарактеризована значениями о - электронных зарядов атомов, но что в общем а-электронное распределение не должно играть ориентирующей роли в реакциях замещения, свойственных ароматическим соединениям. [12]
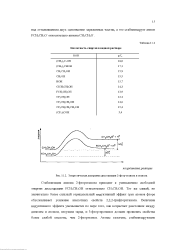 |
Кислотность спиртов в водном растворе. [13] |
Тот же самый, но значительно более сильный отрицательный индуктивный эффект трех атомов фтора обусловливает усиление кислотных свойств 2 2 2-трифгорэтанола. Величина индуктивного эффекта уменьшается по мере того, как возрастает расстояние между диполем и атомом, несущим заряд, и 3-фтор-пропанол должен проявлять свойства более слабой кислоты, чем 2-фгорэтанол. [14]
Тот же самый, но значительно более сильный отрицательный индуктивный эффект трех атомов фтора обусловливает усиление кислотных свойств 2 2 2-трифторэтанола. Величина индуктивного эффекта уменьшается по мере того, как возрастает расстояние между диполем и атомом, несущим заряд, и 3-фтор-пропанол должен проявлять свойства более слабой кислоты, чем 2-фторэтанол. Атомы галогена, стабилизирующие алкоксид-ион, обладают - / - эффектом, а алкилъные группы, дестабилизирующие алкоксид-ион, обладают / - эффектом. Другое возможное объяснение более низкой кислотности дареда-бутилового спирта, не связанное с проявлением / - эффекта метильных групп, состоит в том, что отрет-бутильная группа создает сильные стери-ческие препятствия для образования прочной межмолекулярной водородной связи. Если образование сильной межмолекулярной водородной связи в растворе играет решающую роль в диссоциации воды, спиртов и других О - Н - кислот ( гл. [15]
Страницы: 1 2