Развитие - реакция
Cтраница 1
Развитие реакции приводит к расширению распределения макромолекул по размерам и сложности, а чем более сложна молекула, тем выше содержание в ней полярных групп, тем менее совместима она с исходными менее полярными олигомерами и мономерами. Это может приводить к микрорасслоению системы, еще более усиливающемуся из-за внутримолекулярного сшивания больших макромолекул. Таким образом, и поликонденсационным системам такого типа может быть присуще явление микросинере-зиса, хорошо известное для полимеризациоиного типа формирования сетчатых полимеров. [2]
Развитие реакций ( 26), ( 27) и переход растворимых окислов из шлака в металл создает совершенно недопустимым присутствие большинства окислов и шлаков при сварке титановых и алюминиевых сплавов. Для сварки подобных сплавов используют бескислородные флюсы, которые составляют из солей металлов ( CaF2; KF; NaF; KC1; Nad), или инертные газы. [3]
Развитие реакций ( 15), ( 16) и переход растворимых окислов из шлака в металл делают совершенно недопустимым присутствие большинства окислов и шлаков при сварке титановых и алюминиевых сплавов. Для сварки подобных сплавов используют бескислородные флюсы, которые составляют из солей металлов ( Сар2, KF, NaF, KC1, NaCl), или инертные газы. [4]
Развитие реакций в твердой фазе через перемещение более или менее узкой реакционной зоны - явление, по-видимому, достаточно распространенное и может реализовываться в самых неожиданных ситуациях. [5]
Развитие реакции вправо требует еще более высокой температуры и высокой концентрации СО в газовой фазе. [6]
Развитие реакции ( 3) нежелательно, так как при этом содержание фосфора в шве возрастает, что приводит к снижению его ударной вязкости и повышению порога хладноломкости. [7]
Развитие реакции сшивания можно легко продемонстрировать с помощью следующего эксперимента. Через 5 мин раствор, обработанный S2C12, становится заметно более вязким, чем необработанный, а спустя 10 мин он превращается в гель. Через 20 мин образуется плотная желе-подобная масса. Еще через несколько часов степень сшивания уже настолько велика, что происходит разделение фаз с выделением растворителя в результате синерезиса. [8]
Развитие реакции образования макромолекул при этом, как и в кислой среде, может идти по трем путям. Однако при третьем пути - образовании эфирных связей - реакция сильно заторможена и наблюдается только при температуре выше 130 - 150 С. [9]
Развитие реакций горения газов идет, подчиняясь особым характерным закономерностям, при этом возникают цепные реакции. Взаимодействие образовавшихся активных центров ( О, Н и ОН) со стабильными молекулами не требует большой энергии активации 3, возникающей при горении от нагрева газовоздушной смеси до температуры воспламенения и выше. [10]
Развитию реакции могут способствовать не только фотоны, но и быстрые электроны. Последние оказывают активирующее действие на развитие химической реакции, когда она протекает в электрическом разряде. При соударении быстрого электрона с молекулой энергия поступательного движения электрона превращается во внутреннюю энергию молекулы, которая становится возбужденной. Возбужденная молекула диссоциирует на нейтральные атомы, радикалы или ионы. Теория возбуждения электронным ударом сложна и поэтому не может быть здесь приведена. [11]
Развитию реакции способствуют загрузка мелассы, подогретой до 50 - 60: С. [12]
Развитию реакции окисления в промышленных масштабах сильно мешало распространенное мнение о том, что конечным продуктом реакции должны являться искусственные кислоты, по своим свойствам близкие к кислотам, выделенным из животных и растительных жиров. [13]
Такое развитие реакции в газовом объеме приводит к воспламенению газа, к рождению пламени. [14]
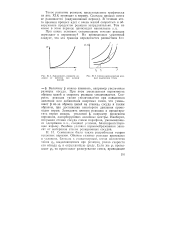 |
Зависимость скорости реакции от времени при цепном взрыве.| Схема расположения кривых выделения тепла. [15] |
Страницы: 1 2 3 4
