Дальнейшее развитие - реакция
Cтраница 2
Стадия 1 наиболее медленная и совершается по первому порядку. Без прохождения этой стадии дальнейшее развитие реакции невозможно. [16]
При этом образуется смесь только мононитросоединений, которые подвергают фракционированию. Процесс зтот представляет по существу дальнейшее развитие реакции Коновалова. [17]
При этом образуется смесь только мононитросоединений, которые подвергают фракционированию. Процесс этот представляет по существу дальнейшее развитие реакции Коновалова. [18]
Длина цепи зависит от соотношения между числом цепей, возникающих в единицу времени, и числом цепей, ликвидирующихся в тот же промежуток времени - обрывающихся. Каждый обрыв цепи уменьшает возможность дальнейшего развития реакции, и при неблагоприятных соотношениях это может привести к полному прекращению ее. [19]
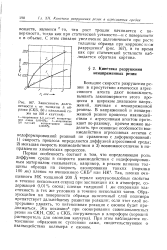 |
Зависимость долговечности т от толщины h об. [20] |
Так, пленки очищенного НК толщиной 200 А теряли каучукоподобные свойства в течение нескольких секунд при экспозиции их в атмосфере, содержащей 0 01 % озона; пленки толщиной 1 мк сохраняли эластичность в тех же условиях в течение нескольких часов. Образующийся на поверхности образца окисленный слой полимера препятствует дальнейшему развитию реакции; если этот слой непрерывно удалять, то интенсивная реакция с озоном будет продолжаться. При этом наблюдается интенсивное образование суспензии сажи, свидетельствующее о / взаимодействии полимера с озоном. [21]
Очевидно, что в зонах деформации с tK tign механически инициированные реакции, выделяя тепло, создают условия и для термического распада ВВ. Тогда, при соответствующих размерах зоны начальной деформации, дальнейшее развитие реакции в ГТ и за пределами будет связано с закономерностями кинетики термораспада. Авторами работы [7.36] была предложена более простая дислокационная модель возбуждения ГТ на искажениях кристаллической решетки за счет аннигиляции дислокаций с антипараллельными векторами Бюргерса. [22]
 |
Пространственная диаграмма состояния тройной системы с эвтектикой.| Плоская диаграмма состояния тройной системы с эвтектикой. [23] |
Результатом этого является образование реакционных ядер, за счет роста к-рых происходит дальнейшее развитие реакции. [24]
 |
Химические реакции металлического урана. [25] |
Причина таких изменений скорости не ясна, однако она может быть связана с распадом при более высоких температурах первоначально образованной окисной пленки. В отличие от алюминия и магния, окисная пленка, которая образуется на металлическом уране, не является плотной и не оказывает защитного или задерживающего действия от дальнейшего развития реакции. [26]
Воздействие самого металла на многостадийный процесс вероятнее всего сосредоточено не на первой, а на последующих стадиях, в которых наличие распыленного металла в объеме может способствовать дезактивации активных частиц, образующихся при взрывном распаде перекиси. Таким образом, наряду с уменьшением начальной концентрации активных центров, с которой начинается вторая стадия низкотемпературного процесса при добавке антидетонатора, последний усиливает, кроме того, уничтожение активных центров при дальнейшем развитии реакции. [27]
С другой стороны, исследования, проведенные в кашей лаборатории 1 ще в 1938 г. [6], показали, что некоторые вещества, известные как активные замедлители окисления нефтяных масел ( фенил - - нафтил-амнн, гидрохинон, резорцин, ос-нафтол, п-оксидифениламин), не обнаруживают сколько-нибудь значительного и отчетливо выраженного в одном определенном направлении действия на термический распад гидроперекиси тетралина, либо совсем не влияют на него, но чрезвычайно активно тормозят первоначальное образование этой гидроперекиси при автоокислоппи тетралина при низкой температуре, при которой гидроперекись устойчива. Из этих наблюдений был сделан вывод, что исследованные замедлители автоокисления углеводородов действуют скорее на реакцию первичного возникновения гидроперекисей ( в индукционном периоде), чем на распад уже образовавшихся гидроперекисей в ходе дальнейшего развития реакции. Предположения, чго замедлители влияют на окислительный процесс в стадии его инициирования, высказываются в последнее время все чаще. [28]
 |
Зависимость выхода формальдегида от содержания NO в метано-воздушной смеси при 650 С.| Кинетические кривые расходования метанола и накопления продуктов окисления. [29] |
Зависимость выхода формальдегида от содержания оксида азота ( II) ( рис. 23), указывает на наличие предела эффективного действия, характерного для инициаторов цепной реакции. Сопоставление кривых расходования метана ( рис. 24) приводит к заключению, что при окислении очень быстро устанавливаются стационарные концентрации формальдегида и метанола. По мере дальнейшего развития реакции происходит лишь накопление больших количеств оксида углерода, во много раз превосходящих содержание и метанола, и формальдегида. [30]
Страницы: 1 2 3