Разделение - ион - металл
Cтраница 1
Разделение ионов металлов является, как правило, результатом совместного действия двух факторов - избирательности ионного обмена и избирательности комплексообразования в растворе. Большинство ионов металлов в водном растворе взаимодействуют с общими анионами с образованием комплексов, и реакция сдвигается в сторону образования комплексов при добавлении неводных растворителей, понижающих диэлектрическую проницаемость. [1]
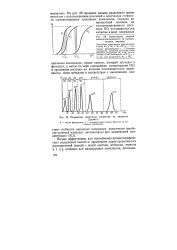
Разделение ионов металлов экстракцией комплексов с ацетил-ацетоном интенсивно исследовалось Ридбергом [22]; результаты его исследований представлены на рис. 3.1. Органической фазой могут служить бензол, хлороформ или гексон. [3]
Разделение ионов металлов на эти две категории не абсолютно, и существуют ионы металлов с пограничными свойствами; тем не менее классификация умышленно сделана резкой и, очевидно, является довольно полезной. Основания также удобно разделить на две категории, а именно те, которые способны к поляризации, или мягкие, и те основания, которые не поляризуются, пли жесткие. Основание может быть мягким и обладать большой склонностью к присоединению протона, например сульфид-ион. Однако в общем правильно, что жесткость основания связывают с - четко выраженной тенденцией к присоединению протона. Например, для оснований, в которых координирующий атом является элементом V, VI и VII групп ( подавлякщее большинство всех оснований), атомы фтора, кислорода и азота - наиболее жесткие в каждой из групп и вместе с тем обладают наибольшей основностью по отношению к протону. [4]
Разделение ионов металлов на анионообменнике осуществляется благодаря селективному образованию анионных комплексов. Список соединений, образующих комплексы с металлами, включает НС1, HF, HBr, HI, HSCN, H2SO4 и Н2О2 ( гл. Удачные разделения металлов проведены при использовании хлористоводородной кислоты. Она является очень подходящей средой, поскольку растворяет многие металлы. [5]
Разделение ионов металлов, содержащихся в жидких промыш-енных отходах, удобно проводить методом реагентной улыпра-шлыпрации. Реагенты, способствующие агрегации извлекаемых онов, повышают задерживающую способность мембран. [6]
Для разделения ионов металлов в виде гидрокси-дов широко используют изменение рН раствора. На рис. 26.6 приведены области рН, при которых осаждаются металлы в виде гидроксидов. [7]
При разделении ионов металлов методом ио-нофореза пластинку промывают водой, обрабатывают парами аммиака и погружают на 10 мин в реактив. При обнаружении разделенных компонентов на тонкослойной хроматограмме пластинку опрыскивают сначала реакти-вом, а затем 25 % - ным раствором аммиака. [8]
Большинство методик разделения ионов металлов на иони-тах основано на различии в устойчивости их комплексных соединений. Комплексообразующие реагенты или анионы можно использовать в качестве противоионов для смол, их можно вводить в растворы, из которых ведется сорбция, или использовать для десорбции удержанных катионов. Меняя величину рН, комплексообразующий реагент и его концентрацию, можно в значительных пределах менять устойчивость комплексов и тем самым увеличивать различия в константах распределения, а в итоге повышать степень разделения. [9]
Очень эффективным способом разделения ионов металлов является ионообменное разделение хлоридных комплексов. Из растворов соляной кислоты извлекаются многие ионы металлов; оптимальная концентрация НС1 зависит от природы извлекаемого иона. В большинстве случаев с ростом концентрации кислоты извлечение сначала растет до некоторого максимального значения, а затем падает. При высокой концентрации кислоты добавляемые хлорид-ионы начинают конкурировать за активные центры смолы даже с устойчивыми анионными комплексами металлов. К немногим металлам, которые практически не сорбируются из хлоридных растворов, относятся щелочные, щелочноземельные, редкоземельные элементы и никель. [10]
 |
Разделение К и Mg2 на ка. [11] |
Очень широко используется способ разделения ионов металлов путем их превращения в анионные комплексы, которые значительно различаются по устойчивости и вследствие этого в разной степени поглощаются анионитом. FeClI в значительной степени диссоциирован. [12]
Таким образом, прогнозирование разделения ионов металлов на ионитах, модифицированных каким-либо органическим реагентом, может быть сведено к определению констант устойчивости комплексов разделяемых элементов с данным реагентом. Для разделения следует выбирать те значения рН, при которых разница в константах устойчивости комплексов разделяемых элементов наибольшая. [13]
На рис. 59 приведен пример разделения ионов металлов с использованием различий в константах стойкости соответствующих хлоридных комплексов. [15]
Страницы: 1 2 3 4