Разделение - кобальт
Cтраница 2
В заключение следует остановиться на катионитах с карбоксильными группами [48 ] и на хелатных катионитах, которые также применяются для разделения металлов рассматриваемых групп. Известен метод разделения кобальта и никеля с помощью хелатных катионитов [18]; следует, однако, иметь в виду, что разделение этих металлов легко и точно осуществляется с помощью анионитов в солянокислой среде. Тем не менее, использование хелатных катионитов имеет определенные преимущества в тех случаях, когде анализируемый раствор содержит анионы или неэлектролиты, мешающие определению этих металлов. Индуцированная радиоактивность натрия-24 и фосфора-32 маскирует у-сцинцияляционные пики слабо радиоактивных веществ. Анализируемый раствор при рН 5 пропускают через колонку с катионитом дауэкс А-1 в Na-форме; затем колонку промывают раствором нерадиоактивного хлорида натрия. [16]
Методы выделения кобальта электролизом и его отделение от других элементов рассмотрены на стр. Был предложен метод разделения кобальта и цинка [339], основанный на выделении обоих элементов на ртутном катоде и последующем анодном растворении полученной амальгамы. При этом цинк переходит из амальгамы в виде ионов в водный раствор, а кобальт выделяется из амальгамы с большим перенапряжением и поэтому практически полностью остается растворенным в ртути. Проверка метода показала [39], что разделение не количественно, много цинка остается в амальгаме. [17]
В заключение следует отметить, что использование карбоно-вых кислот как экстрагента для извлечения металлов из кислых растворов, в промышленных условиях весьма ограничено. То, что порядок разделения кобальта от никеля из кислых растворов карбоновыми кислотами обратный по отношению к Д2ЭГФК, дает основания для их использования при соответствующих условиях. Во всех других случаях экстракции металлов из кислых растворов является более эффективным экстр агентом. [18]
Были проведены также опыты по разделению кобальта, никеля, марганца, меди, цинка. Разделение этих элементов основано на различной устойчивости анионных хлоридных комплексов в растворе соляной кислоты. [19]
Часто для отделения никеля и других элементов сероводородным методом используют маскирующие вещества. Свифт и Бартон [1209, 1211] рекомендуют для разделения кобальта, никеля, цинка, железа, хрома, алюминия и марганца вести осаждение в присутствии оксалата и бикарбоната натрия. При этом три последние элемента остаются в растворе. [20]
Неправильный выбор растворителя в ряде случаев может сделать разделение невозможным. Можно показать, что если бы для разделения кобальта и железа использовался какой-нибудь активный растворитель, например бутиловый спирт, то оно было бы неосуществимо. [21]
Экстракционное и промывочное действие колонны прак чески не зависит от диаметра колонны. В колоннах диаметрг 5 и 56 см одной и той же высоты разделение кобальта и нике одинаково. Однако необходимая высота колонны зависит температуры экстракции и уменьшается при повышении ее 60 С. [22]
Насколько можно видеть из такого краткого обзора свойств элементов подгруппы железа и методов их обнаружения и определения, железо довольно резко отличается от сходных между собой кобальта и никеля. Это делает малоинтересным изучение и разработку хроматографических методов отделения железа от кобальта и никеля и, наоборот, определяет целесообразность хроматографических методов разделения кобальта и никеля. И хотя, как правило, специальные работы по разделению смесей кобальта и никеля методом ионообменной хроматографии в литературе практически отсутствуют, этот вопрос обсуждается как частный случай в довольно большом числе статей; краткое содержание некоторых из них и приводится ниже. [23]
Для разделения кобальта и никеля были применены колонки из 8-оксихинолина, нафтахинолина и купферона. Полученная константа является функцией как химических свойств сорбируемого иона, так и свойств сорбента. Эти исследования были продолжены В. В. Кулебакиной и Е. И. Са вельевой, осуществившими полное хроматографическое разде - Ч 1ление тартратных комплексов кобальта и никеля на окиси Чалюминия. [24]
Это очень большое количество ступеней, используемое в промышленной практике. Использование ситчатой пульсационной колонны для разделения кобальта от никеля Д2ЭГФК, вероятно, позволит достичь тех же результатов [ 71 при меньших затратах. [25]
Разделение двух металлов со сходными свойствами, как правило, обходится дороже экстракции одного металла ( например, и правильный выбор экстракционной системы является: фактором в определении наиболее экономичного варианта. Выбор экстракционной системы зависит от свойств водной системы, природы и содержания анионов. Для подтверждения этого положения ниже приводится описание методики выбора оптимального варианта экстракции и разделения кобальта от никеля из сернокислых растворов. [26]
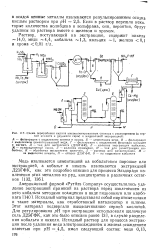 |
Схема переработки скрапа высоколегированных сплавов с растворением ( в серной кислоте и двуокиси серы и жидкостной экстракцией. [27] |
Исходный матер нал представлял собой пир итные шлаки и такие материалы, как отработанный катализатор и шламы. Для регулирования рН при экстракции использовали щелочную соль Д2ЭГФК, как это было описано ранее [3], в случае разделения кобальта и никеля. [28]
Частично обезвоживаясь уже при обычной температуре, СоСЬ - бНаО приобретает в зависимости от степени влажности воздуха ту или иную окраску. При повышенной температуре потеря ионом кобальта части связанной с ним воды происходит даже в растворе, что и сопровождается изменением цвета последт него при нагревании. Различное отношение СоСЬ - НаО и NiCla-HjO к ацетону ( в котором первая соль растворима хорошо, а вторая почти нерастворима) может быть использовано для разделения кобальта и никеля. [29]
Страницы: 1 2 3