Разделение - лантанид
Cтраница 2
Химически наиболее устойчивым является трехвалентное состояние америция. В этом состоянии америций очень схож с лантанидами, которые и используются поэтому как инертные носители при выделении америция. При катионообменном разделении лантанидов и америция последний вымывается из колонны лимоннокислыми солями рядом с прометием. [16]
Для этой цели берут полученную дробной кристаллизацией фракцию, содержащую только смесь Tm Yb или Lu Yb, которую методом кристаллизации уже не удается разделить. Затруднений, встречавшихся при разделении лантанидов классическими методами и обусловленных большим сходством солей трехвалентных лантанидов, сразу удается избежать путем превращения одного из элементов в соединения другой степени окисления, в которых они обладают иными химическими свойствами. [17]
Возможности метода ионного обмена очень сильно возрастают при использовании в качестве элюантов комплексообра-зующих реагентов. Если теперь добавить комплексообразующий реагент ( лиганд), который образует комплекс с одним из этих катионов, то концентрация ( активность) последнего сильно понизится, вследствие чего равновесие сместится в сторону адсорбции второго катиона. Именно такой метод был применен для разделения лантанидов, продуктов распада ( разд. [18]
И все элементы ot актиния до лоуренсия имеют практически одинаковые химические свойства, подобно лантану и лантанидам. Трансурановые элементы прекрасно разделяются методом ионообменной хроматографии, аналогично разделению лантанидов. [19]
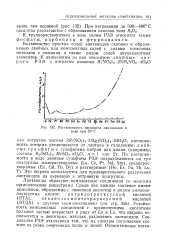 |
Растворимость оксалатов лантанидов в воде при 25 С. [20] |
Лантаниды образуют комплексные соединения со многими органическими веществами. Среди них важное значение имеют комплексы, образуемые с лимонной кислотой и рядом аминопо-лиуксусных кислот: нитрилотриуксусной кислотой ( НТА), этилен д и аминтетрауксусной кислотой ( ЭТДА) и другими комплексонами ( см. стр. Устойчивость комплексных соединений с органическими кислотами большей частью возрастает в ряду от La к Lu, что широко используется в некоторых методах разделения лантанидов. Соединения РЗЭ отличаются тем, что их спектры поглощения состоят из резко очерченных полос и линий. [21]
Дело осложняется еще и тем, что лантаниды образуют комплексы с координационным числом больше шести. Иногда получаются тетракис-комплексы с бидентатными лигандами, причем идентичность строения молекул в различных фактических состояниях часто находится под вопросом. Хотя тетракис-комплексы В-дикетонатолантанидов формально несут один отрицательный заряд, имеются доказательства, что они так же, как и нейтральные трис-комплексы, могут оказаться достаточно летучими для использования в газовой хроматографии. По мере того как мы узнаем о факторах, влияющих на летучесть, становится ясным, что разделение лантанидов методом газовой хроматографии лишь вопрос времени. [22]
Неорганические вещества часто имеют близкие электрофоре-тические свойства, поэтому их разделение в обычных электролитах не дает хороших результатов. Однако образование ионных комплексов часто приводит к изменению электрофоретических свойств центральных ионов, что позволяет провести их разделение. Так, например, согласно данным Джокла [45] и Джокла, Андейча и Майера [47], путем правильного подбора лиганда и рН методом зонного электрофореза в лигандном буферном растворе удалось разделить такие близкие ионы, как катионы редкоземельных элементов. Примеры разделения в лигандных буферных растворах и составы этих растворов приведены в табл. 12.12 и на рис. 12.21. Применяемые лиганды - это анионы неорганических и органических кислот. Щавелевая кислота применяется для разделения Th, LJ и Ра, а гликолевая - разделения лантанидов, Th, U, Zr, обычных катионов и редкоземельных элементов. [23]
Самый старый метод фронтальной хроматографии обладает лишь немногими преимуществами. Лучшие результаты дает вытеснительная хроматография, однако наиболее эффективен метод проявительной хроматографии. Небольшое количество смеси ионов В и С, обладающих большим сродством к иониту, вводят в колонку вместе с ионами А, обладающими малым сродством к иониту. Величина вводимой пробьв пренебрежимо мала по сравнению с полным объемом колонки - Элюирование ведут ионами А. Коэффициент распределения - это отношение концентраций ионов в ионообменной фазе и в растворе, отнесенное к миллилитру раствора и к грамму ( сухой массы) или миллилитру ионообменной фазы. При слишком большом Ка, например более 30, хроматографические зоны расширяются и увеличивается время, необходимое для разделения. Степень сшивки ионитов должна быть достаточно высокой, чтобьь их объем оставался неизменным, или это должны быть макропористые иониты. Благоприятное действие оказывает увеличение скорости потока элюента в колонке, способствующее более равномерному распределению пленки жидкости по поверхности зерен ионита, но слишком сильное увеличение скорости может увести систему из оптимального равновесного состояния. Величины коэффициентов распределения зависят от состава элюента, и их можно регулировать в значительных пределах, добавляя комплексообразующие компоненты; например, при разделении лантанидов с этой целью используют органические оксикислоты. [24]
Ионный обмен позволяет удалять из раствора нежелательные ионы и электролит, заменять их другими или отделять друг от друга. Когда электролит протекает через колонку, он обменивает свои противоионы на противоионы, содержащиеся в зернах ионита. Поэтому вытекающий из колонки раствор содержит до проскока только противоионы, вытесненные из зерен ионита. Степень отработки ионита зависит от размеров колонки, положения равновесия ионного обмена, химического состава ионита и условий работы колонки. Если ионит селективно поглощает противоионы из раствора, то между зонами обоих сортов противоионов возникает и сохраняется острый фронт, который делается стационарным. Иониты в Н - и ОН-форме могут полностью освободить растворы от содержащихся в них катионов и анионов. Необходимо умело использовать избирательное действие различных ионитов, содержание в них различных функциональных групп и различный характер связи их с противоионами металлов или анионами. Большое значение имеет применение процессов комплек-сообразования для разделения смесей ионов. Эти разделения основаны на образовании комплексных соединений металлов с одним комплексообразователем, но различающихся величинами констант нестойкости. Очень эффективно разделение лантанидов и актинидов, основанное на комплексообразовании с анионами органических кислот: винной, лимонной, комплексонов различного состава и других. [25]
Страницы: 1 2