Разделение - ионизированное неионизированное вещество
Cтраница 1
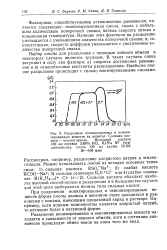 |
Разделение ионизированных и неионизированных веществ на ионитах. Соляная кислота - этиленгликоль. Исходный раствор 100 мл состава 3 65 / о НС1, 6Д5 / о ЭГ ( эти. [1] |
Разделение ионизированных и неионизированных веществ находится в зависимости от ионного обмена, хотя в состоянии равновесия происходит обмен ионов на ионы того же вида. [2]
Теория разделения ионизированных и неионизированных веществ с помощью ионного обмена подробно описана Витоном и Бауманом ( 131, а также Симпсоном и Витоном И2 ] и подробно обсуждается Витоном и Бауманом в главе VII настоящей книги. [3]
При разделении ионизированных и неионизированных веществ на ионитах, как и при наиболее близкой к нему ионообменной хроматографии, аппаратом, где происходит разделение, является колонна, заполненная частицами ионообменной смолы в: качестве насадки с пустотами, заполненными водой или раствором. Если через заполненную таким образом смолой и водой колонну проходит раствор, содержащий два каких-то растворенных вещества ( А и В), то они появятся в потоке, вытекающем из колонны, в различное время, если их коэффициенты распределения различны. [4]
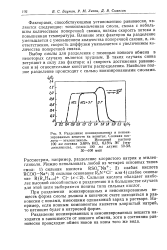 |
Разделение ионизированных и неионизированных веществ на ионитах. Соляная кислота - этиленгликоль. Исходный раствор 100 мл состава 3 65 / о НС1, 6Д5 / о ЭГ ( эти. [5] |
При разделении ионизированных и неионизированных веществ форма смолы должна в конечном счете находиться в равновесии с ионами, имеющими одинаковый заряд в растворе. Например, если ионным компонентом является хлористый натрий, то катионит будет в натриевой форме. [6]
При разделении ионизированных и неионизированных веществ на ионитах, как и при наиболее близкой к нему ионообменной хроматографии, аппаратом, где происходит разделение, является колонна, заполненная частицами ионообменной смолы в: качестве насадки с пустотами, заполненными водой или раствором. Если через заполненную таким образом смолой и водой колонну проходит раствор, содержащий два каких-то растворенных вещества ( А и В), то они появятся в потоке, вытекающем из колонны, в различное время, если их коэффициенты распределения различны. [7]
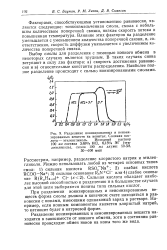 |
Разделение ионизированных и неионизированных веществ на ионитах. Соляная кислота - этиленгликоль. Исходный раствор 100 мл состава 3 65 / о НС1, 6Д5 / о ЭГ ( эти. [8] |
При разделении ионизированных и неионизированных веществ форма смолы должна в конечном счете находиться в равновесии с ионами, имеющими одинаковый заряд в растворе. Например, если ионным компонентом является хлористый натрий, то катионит будет в натриевой форме. [9]
Вообще, метод разделения ионизированных и неионизированных веществ может применяться для отделения любого ионного, растворимого в воде вещества от любого неионного растворимого вещества с низким молекулярным весом. Соли, кислоты и основания могут быть отделены от целого ряда слабых кислот, аминов, спиртов, аминокислот кетонов, альдегидов и даже неорганических соединений, например аммиака и борной кислоты. Этот метод весьма пригоден для аналитических определений. [10]
При развитии процесса разделения ионизированных и неионизированных веществ очень быстро было установлено, что наиболее полная степень использования смолы достигается в том случае, когда между ионными и неионными фракциями имеется возможно меньше чистой воды, и что при чередовании исходного раствора и воды в соответствующем соотношении можно осуществить полунепрерывный процесс. [11]
Вообще, метод разделения ионизированных и неионизированных веществ может применяться для отделения любого ионного, растворимого в воде вещества от любого неионного растворимого вещества с низким молекулярным весом. Соли, кислоты и основания могут быть отделены от целого ряда слабых кислот, аминов, спиртов, аминокислот кетонов, альдегидов и даже неорганических соединений, например аммиака и борной кислоты. Этот метод весьма пригоден для аналитических определений. [12]
При развитии процесса разделения ионизированных и неионизированных веществ очень быстро было установлено, что наиболее полная степень использования смолы достигается в том случае, когда между ионными и неионными фракциями имеется возможно меньше чистой воды, и что при чередовании исходного раствора и воды в соответствующем соотношении можно осуществить полунепрерывный процесс. [13]
Как уже было показано, разделение ионизированных и неионизированных веществ возможно в том случае, если растворенные вещества имеют достаточно различные коэффициенты равновесного распределения. Способность к разделению ионизированных и неионизированных веществ определяется различием коэффициентов распределения. Например, разделяющая способность для получения гликоля из раствора с 10 % соли и 10 % гликоля с помощью цикличного метода разделения ионизированных и неионизированных веществ, как показано на лабораторном опыте, отраженном на рис. 12, находится в пределах 22 кг гликоля на 1 м3 смолы в час. На разделяющую способность мало влияет изменение концентрации соли до 20 %, но это является функцией первоначальной и конечной концентраций гликоля. [14]
Выше было дано лишь простое описание разделения ионизированных и неионизированных веществ с помощью ионного обмена. При возможном применении этого процесса рассматриваются и такие вопросы, как размер молекул. [15]
Страницы: 1 2