Разделение - смесь - аминокислота
Cтраница 3
Между тем разделение смеси аминокислот, изолирование из смеси каждой из них встречаются с рядом затруднений, так как физические и химические свойства многих аминокислот довольно сходны. [31]
В связи с неодинаковым аминокислотным составом гидролизатов различных белков приходится несколько менять и условия их разделения. Вопрос о применении ионообменивающих смол для разделения смесей аминокислот находится еще в начальной стадии разработки. Однако уже и теперь достаточно отчетливо намечаются области их использования не только в химии белка, но и во многих других разделах биохимии. [32]
Таким образом, в зависимости от рН среды поведение различных групп аминокислот будет различным, их ионы будут обладать разным знаком и числом зарядов. Это свойство и позволяет применять ионообменники для разделения смеси аминокислот. [33]
Если набить стеклянную трубку мелкозернистым ( с подходящей степенью-дисперсности) сульфированным полистиролом ( или, как принято говорить, смолой) и пропустить через нее кислый нитратный буфер с рН 3 25, то получится ионообменная колонка анализатора. При проведении анализа на поверхность смолы в колонке наливают раствор подлежащей разделению смеси аминокислот ( или обработанный гидролизат белка), и пропускают цитратный буфер, в результате чего начинается процесс хроматографирования, состоящий в том, что ионы аминокислот, проходя по колонке вместе с буфером, будут периодически вытеснять катионы, присоединенные к сульфогруппам, или сами вытесняться свободными катионами. [34]
На целлюлозе ( или крахмале) в виде полоски или колонны происходит разделение смеси аминокислот вследствие различной относительной растворимости ( коэффициентов распределения) и адсорбируемости индивидуальных аминокислот в воде, неподвижно удерживаемой носителем, и в несмешивающемся с водой растворителе, который медленно движется вдоль бумажной ( или крахмальной) колонны за зоной, содержащей всю смесь аминокислот. [35]
 |
Элюцйонное разделение аминокислот на крахмальной колонке ( по. [36] |
Этот метод называется проявительным. На рис. VI, 4 приведена типичная дифференциальная хроматограмма, полученная при разделении смеси аминокислот на колонке с крахмалом. Как можно видеть, почти каждый компонент дает на кривой самостоятельный пик и может быть собран в отдельную фракцию. [37]
К началу работы Фишера была известна примерно дюжина аминокислот, как продуктов расщепления белков, другие были открыты немного позже. Фишер начал работать по нескольким направлениям: синтез аминокислот и расщепление их рацемических форм; исследования производных аминокислот для того, чтобы ускорить разделение смесей аминокислот и, что особенно важно, рекомбинация двух или более аминокислот в вещества, которые он назвал полипептидами. Величие фишеровского подхода к проблеме полипептидного синтеза произвело прямое воздействие и было склонно затмить другие пионерские работы в этой области, такие как работы КурЦиуса. В 1901 г. он объявил о синтезе гли-цил-глицина - простейшего дипептида, а в 1907 г. - о 18-ти членном полипептиде лейцил-триглицил-лейцил-триглицил - лейцил-окта-глицил-глицина. [38]
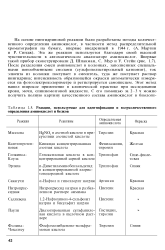 |
Реакции, используемые для идентификации и полуколичественного определения аминокислот и белков. [39] |
На основе нингидриновой реакции были разработаны методы количественного определения аминокислот, в частности метод распределительной хроматографии на бумаге, впервые внедренный в 1944 г. ( А. Эта же реакция используется благодаря своей высокой чувствительности в автоматическом анализаторе аминокислот. После разделения смеси аминокислот в колонках, заполненных специальными ионообменными смолами ( сульфополистирольный катионит), ток элюента из колонки поступает в смеситель, туда же поступает раствор нингидрина; интенсивность образующейся окраски автоматически измеряется на фотоэлектроколориметре и регистрируется самописцем. [40]
Максимально на пластинку следует наносить 1 - 2 мкг смеси аминокислот. При разделении смеси аминокислот с близкими значениями Rf для получения воспроизводимых результатов допустима 4 - 5-кратная разница в их концентрациях. Когда Rf аминокислот сильно различаются, это, конечно, не имеет значения. [41]
Это обусловлено, по всей вероятности, тем, что в белковой молекуле некоторые реактивные группы скрыты внутри глобулы и вследствие этого недоступны действию окрашивающего реагента ( см. гл. Поэтому для определения аминокислотного состава белка необходимо подвергнуть его полному гидролизу. Разделение смеси аминокислот представляет собой трудную задачу, так как аминокислоты являются амфолитами, растворимыми в воде и нерастворимыми в таких органических растворах, как спирт. Только иминокислоты пролин и окси-пролин растворимы в этиловом спирте. Ввиду того что аминокислоты обладают сходными физико-химическими свойствами, их нельзя разделить фракционированием спиртом или нейтральными солями. [42]
Аминокислоты и пептиды представляют собой гидрофильные соединения, трудно растворимые в безводных жидкостях. Обычно разделение этих соединений проводят на слое силикагсль - гипс. Возможно также хроматографиро-вание аминокислот в виде солей, но в этом случае применяют буферные слои силикагеля. Для разделения смесей аминокислот, пептидов и протеинов был использован слой сефадекс G-25, так называемый гельфильтр ( стр. [43]
Таким образом, ясно, что для того, чтобы попытаться решить-проблему химического строения белка, необходимо было обладать известным мужеством и исключительным мастерством экспериментатора. Наметив основные направления исследований, он начал неутомимо и последовательно осуществлять свою программу. Изучив свойства и методы синтеза тех аминокислот, которые обнаруживали в белковых гидро-лизатах, он разработал метод разделения смесей аминокислот и использовал его для выделения и идентификации отдельных аминокислот из смесей продуктов кислотного, щелочного или ферментативного разложения белков. [44]
Сначала получается гидрохлорид эфира, при добавлении основания эфир аминокислоты освобождается, извлекается органическим растворителем и перегоняется в вакууме. Свободные эфиры имеют характерный аминный запах. При хранении и особенно при нагревании они переходят в 2 5-дио-ксопиперазины, отщепляя спирт. По этой же причине часть продукта теряется при перегонке эфиров аминокислот. Относительно термически устойчивы изопропиловые эфиры, и благодаря этому свойству они были предложены для осторожного разделения смесей аминокислот перегонкой их эфиров. [45]
Страницы: 1 2 3 4