Разделение - алкалоид
Cтраница 3
Смола с высокой механической прочностью н относительной устойчивостью к действию радиации; селективно поглощает цезий. Используется для разделения алкалоидов. [31]
Количественное определение берберина пектрофотометрическим методом с приме-е н и е м хроматографии в то к ком слое с о р-е н т а. Метод основан па разделении алкалоидов в тонком слое) рбента и определении содержания берберина спектрофотометри-жким методом. [32]
Очастш извлечений хроматографическим методом ( на коло / да Адсорбционная хроматография основана на избирательной адсо): ции одного или нескольких веществ из - растворов или из парогаЕ образной смеси твердыми веществами - сорбентами ( адсорбентам. Хроматографический метод очистки и разделения алкалоидов пр меним как к водным растворам солей алкалоидов, так и к растЕ рам оснований алкалоидов в органических растворителях, Адсор цирнные процессы, применяемые в химико-фармацевтической п (: мышлешюсти, делят на две группы: 1) процессы очистки, при ко: рых поглощаются примеси ( сопутствующие вещества), а алкалои, остаются в растворе; 2) процессы очистки, при которых поглощают алкалоиды, а сопутствующие вещества остаются в растворе. [33]
Затем этот метод был применен для разделения алкалоидов ( Хорнинг), и в первую очередь группы папаверина. [34]
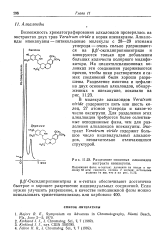 |
Разделение основных алкалоидов экстракта ипекакуаны. [35] |
В молекуле алкалоидов Veratrum viride содержится пять или шесть колец, 27 атомов углерода и какое-то число оксигрупп. Для разделения этих алкалоидов требуются более селективные неподвижные фазы, чем для разделения алкалоидов ипекакуаны. Экстракт Veratrum viride содержит большое число индивидуальных алкалоидов, незначительно отличающихся структурой. [36]
В некоторых случаях более качественные разделения осуществляются в темноте, как, например, разделение алкалоидов раувольфии [17], а количественное определение таких фоточувствительных веществ обязательно проводится в темноте или при слабом освещении. [37]
Для разделения алкалоидов на колонке с каолином рекомендуют использовать в качестве элюанта воду. [38]
 |
Техника бумажной хроматографии. [39] |
Возможность разделения малых количеств веществ, простота эксперимента и разнообразие экспериментальных условий позволяют использовать бумажную хроматографию почти во всех областях химического исследования. Шире всего этот метод применяют в биохимии, например для разделения аминокислот и пептидов при исследовании структуры белков. Метод применяют также для разделения алкалоидов, стероидов и различных экстрактов из природных продуктов. Бумажную хроматографию используют для разделения радиоизотопов. Были предложены способы, позволяющие в полевых условиях обнаруживать и определять металлы в почвах и геологических образцах. [40]
Фостор и сотрудники для разделения алкалоидов спорыньи и одновременно Мюнье и Машбеф [ 3J, которые заложили основы методики для алкалоидов всех типов. В вводной части: той главы будут рассмотрены: общие закономерности, реактивы для проявления, системы растворителей, подготовка проб и количественное определенно, являющиеся общими для алкалоидов различных групп. Конкретные условия опыта, пригодные для разделения химически сходных алкалоидов, будут рассматриваться далее, в специальных разделах. Метилированные ксантипы рассмотрены выше в главе, посвященной иуриповым основаниям ( см. стр. [41]
Помощь в оценке результатов предварительных определений оказывают сведения о температурах плавления алкалоидов ( стр. Алкалоиды, обнаруживаемые в продуктах питания и фураже, приходится экстрагировать и после отделения мешающих определению примесей выделять. Затем применяют весьма распространенный в токсикологическом анализе способ Стаса - Отто. Этот метод разделения алкалоидов на три группы зиждется на различной их основности. Материал пробы измельчают, суспендируют в спирте и после прибавления некоторого количества винной или небольшого количества серной кислоты кипятят 15 мин с обратным холодильником. Смесь после охлаждения фильтруют и фильтрат значительно упаривают на водяной бане. [42]
В случаях, когда алкалоиды в смеси сильно различаются по точкам кипения, их возможно разделить фракционной перегонкой под вакуумом, учитывая, что почти все алкалоиды нетеплостойки и разлагаются при высоких температурах. Чаще пользуются различием растворимости алкалоидов в разных растворителях. В иных случаях удается путем обработки смеси подходящим растворителем перевести в раствор только одно из оснований. В других случаях для разделения алкалоидов можно использовать различную их растворимость в зависимости от температуры, когда за счет этого при последующем охлаждении менее растворимый алкалоид раньше выпадает из раствора. [43]
По такому же методу нами был переработан другой вид травы лобелии - лобелия жгучая [10, 11], отличающийся от лобелии одутлой большим суммарным содержанием алкалоидов. Для их препаративного разделения нами вначале были испытаны целлюлоза и кизельгур, на которых разделение не было достигнуто. Испытание окиси алюминия различных групп активности показало, что лучшее разделение достигается на окиси алюминия третьей группы второй подгруппы. При десорбции хлороформом с колонки, адсорбировавшей сумму двух алкалоидов, мы обнаружили, что алкалоид № 1 значительно лучше растворяется в хлороформе и может быть им полностью вымыт с окиси алюминия. На рис. 2 представлена выходная кривая вытеснения алкалоидов лобелии жгучей с окиси алюминия, отображающая полноту извлечения и четкость разделения алкалоидов на колонке. В результате проведенных опытов нами была разработана методика, позволяющая разделить алкалоиды лобелии жгучей и получить их в кристаллическом виде. [44]
Разделение проводилось на слоях кремневой кислоты и оксида магния, взятых в соотношении 1: 1, связующим служил алебастр. Борке и Кирш показали, как важно замешивать адсорбенты не на чистой воде, а на буферных растворах. Мариани и Мариани-Марелли [109] разделяли опийные алкалоиды на забуференном слое ( рН 5, ацетатный буфер) оксида алюминия. Оксид алюминия активировали при 500 С, после чего адсорбировали на нем 5 % буферного раствора. Экстракты различных опиумов можно разделить таким способом за 15 мин. Пятна наблюдают в УФ-свете. Для обнаружения пятен применяли реактив Драген-дорфа, усовершенствованный Мунье. Описанным способом можно проводить и количественное определение: равномерно опрысканные пластинки фотографируют и затем промеряют пятна. Хойзер [112] определял методом ТСХ различные алкалоиды в лекарственных растениях, а также морфин в порошкообразном опиуме. В работах [113-115] описано разделение опийных алкалоидов методом двумерной хроматографии на оксиде алюминия. [45]
Страницы: 1 2 3