Различие - растворимость
Cтраница 2
Пользуясь различием растворимости солей в жидком МНз и воде, можно иногда осуществлять обращение обычно наблюдаемых реакций ионного обмена. [16]
 |
Растворимость NaCl в жидком аммиаке ( г / 100 г МН3.| Растворимость щелочных.| Электропроводность растворов Na в жидком аммиаке. [17] |
Пользуясь различием растворимости солей в жидком NH3 и воде, можно иногда осуществлять обращение обычно наблюдаемых реакций ионного обмена. [18]
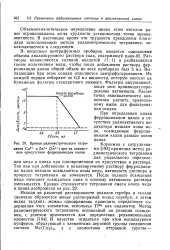 |
Кривая радиометрического титро. [19] |
Исходя из различий растворимости иодидов серебра и таллия ( вначале образуется менее растворимый иодид серебра, а затем иодид таллия), можно одновременно проводить определение со-держация этих элементов, используя Т1204 как индикатор. [20]
В данном случае различие растворимости их солей объясняется тем, что в 1 3-бензолдисульфо-кислоте взаимное влияние двух сульфогрупп, содержащихся в ее молекуле, как известно, невелико, в то время как в молекуле 1 4-дисульфокислоты оно намного больше. [21]
Этот метод построен исключительно на различии растворимости, соответственно летучести. Если имеется достаточная разница в растворимости, то таким образом можно приготовить даже сравнительно легко растворимые соли; правда, для очистки их часто надо еще перекристаллизовать. Известным примером применения этого метода является получение конверсионной селитры ( см. стр. [22]
Этот метод очистки основан на различии растворимости примеси в твердом веществе и в расплаве. Образец твердого вещества ( например, стержень из металла, подлежащего очистке) медленно передвигают через узкую зону нагревания, при этом происходит постепенное расплавление отдельных участков образца, находящихся в данный момент в зоне нагревания. Примеси, содержащиеся в образце, накапливаются в жидкой фазе, вместе с ней передвигаются вдоль образца и по окончании плавки оказываются в конце образца. Как правило, зонную плавку повторяют многократно. Зачастую образец движется через несколько обогреваемых зон, что позволяет в несколько раз сократить время очистки. [23]
В ПП 44 и 46 используется различие растворимости в кислоте сульфидов мышьяка, сурьмы и олова. [24]
Как видно из табл. 15, различия растворимости углеводородных газов относительно невелики. [25]
 |
Характеристические кривые, полученные при сопоставлении различных способов разрушения скрытого изображения. [26] |
Возможность замены анионной подрешетки основана на различии растворимости галогенида серебра исходной и конвертированной эмульсии. [27]
Разделение смеси при помощи экстракции основано на различии растворимости компонентов в воде и в органических растворителях или на различии кислотно-основных свойств. [28]
Разделение жидких смесей селективной экстракцией основано на различии растворимости веществ в двух несмешивающихся жидких фазах. Мерой эффективности, характеризующей способность двух различных растворителей разделять компоненты смеси, служит фактор разделения - отношение коэффициентов распределения веществ между фазами. Под коэффициентом распределения ( К) понимают отношение концентраций ( в моль / л) вещества в органической ( С) и водной ( СВ) фазах. Для практических целей необходимо, чтобы величина фактора разделения находилась примерно в пределах 2 - 10 [64], что обусловливается взаимодействием между компонентами. При сильном взаимодействии между растворителем и растворенным веществом ( фактор разделения больше 10) затрудняется регенерация растворителя и выделение растворенного компонента. Когда компоненты взаимодействуют слабо ( фактор разделения меньше двух), для полного извлечения экстрагируемого вещества из исходной смеси требуется большое число ступеней разделения. [29]
Разделение в газо-жидкостной распределительной хроматографии основано на различии растворимости разделяемых веществ в неподвижном растворителе в хроматографической колонке, или, более точно, на различии коэффициентов их распределения между неподвижной жидкой фазой ( НЖФ), служащей растворителем, и подвижной газовой фазой ( ПГФ), служащей газом-носителем. Чем больше коэффициент распределения, тем больше объем удерживания вещества и тем дольше оно задерживается: в колонке. Коэффициент распределения К равен частному от деления концентрации компонента в НЖФ на концентрацию компонента в ПГФ. Величина К является термодинамической константой равновесия в процессе распределения растворяющегося вещества между НЖФ и ПГФ, подобно тому, как коэффициент адсорбции Г в адсорбционной хроматографии является термодинамической константой в процессе распределения адсорбирующегося вещества между твердой неподвижной фазой - адсорбентом и ПГФ - газом-носителем. [30]
Страницы: 1 2 3 4