Энергетическое различие
Cтраница 2
Ввиду энергетических различий на ориентированных по-разному гранях металла следует ожидать, что и степень адсорбции дисперсных частиц будет разной. [17]
Вследствие небольших энергетических различий между структурами вюртцита и цинковой обманки может наблюдаться и иная последовательность в расположении плотноупакованных слоев с большими периодами повторения. [18]
Увеличение энергетического различия орбиталей уменьшает возможность 5р3 - гибридного состояния. Поэтому, например, в ряду тетра-эдрических ионов SiOj - - РО - - SO - - ClO по мере уменьшения склонности к зр3 - гибридизации валентных орбиталей центрального атома устойчивость ионов понижается. [19]
Для кремнезема энергетическое различие между аморфным и кристаллическим состоянием мало, а перестройка силоксановых связей в системе требует высокой энергии активации. Поэтому золи и гели кремнезема устойчивы и не кристаллизуются. [20]
Тем не менее энергетические различия между указанными типами построения полимерной цепи не столь значительны, чтобы образование менее выгодных последовательностей ( голова-голова или хвост-хвост) оказалось полностью исключенным. [21]
 |
Энергетическое различие ns - и np - уровней атомов р-элементов VI группы и средняя энергия связей в молекулах их гексафторидов. [22] |
В характере изменения энергетического различия ns - и пр-орби-талей в подгруппе проявляется явно выраженная вторичная периодичность. Как видно из табл. 28, энергетическая разность между ns - и np - уровнями для элементов 4-го периода выше, чем для элементов 3-го и 5-го периодов. Следовательно, соединения, отвечающие высшей степени окисления у Зр - и 5р - элементов, должны быть устойчивее, чем у 4р - элементов. [23]
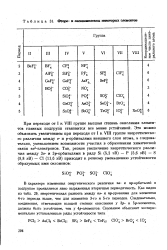 |
Фторо - и оксокошшексы некоторых элементов. [24] |
В характере изменения энергетического различия us - и np - орбиталей в подгруппе проявляется явно выраженная вторичная периодичность. Как видно из табл. 29, энергетическая разность между па - и np - уровнями для элементов 4-го периода выше, чем для элементов 3-го и 5-го периодов. Следовательно, соединения, отвечающие высшей степени окисления у Зр - и 5р - элементов, должны быть устойчивее, чем у 4р - элементов. [25]
 |
Энергетическое различие ns - и np - уровней атомов р-элементов VI группы и средняя энергия связей в молекулах их гексафторидов. [26] |
В характере изменения энергетического различия ns - и пр-орби-талей в подгруппе проявляется явно выраженная вторичная периодичность. Как видно из табл. 28, энергетическая разность между ns - и яр-уровнями для элементов 4-го периода выше, чем для элементов 3-го и 5-го периодов. Следовательно, соединения, отвеяающие высшей степени окисления у Зр - и 5р - элементов, должны быть устойчивее, чем у 4р - элементов. [27]
Автоматическое отражение расчетом энергетических различий структурных изомеров служит лучшим подтверждением правильности рассматриваемого подхода. [28]
Такой процесс возможен из-за относительно малого энергетического различия между возбужденными синглетными состояниями большинства молекул и высокой степени перекрывания их колебательных уровней. После лроцесса внутренней конверсии молекула быстро дезактивируется в результате колебательной релаксации до самого нижнего колебательного уровня состояния Si. Поскольку колебательная релаксация и внутренняя конверсия имеют такие большие скорости, большинство возбужденных молекул в растворе будут переходить на самый нижний колебательный уровень самого низкого возбужденного синглетного состояния до того, как испускается какое-либо аналитически полезное излучение. [29]
 |
Перекрывание валентных орбиталей в молекулах СН, NH3. [30] |
Страницы: 1 2 3 4 5
