Разложение - аммиак
Cтраница 1
Разложение аммиака на вольфраме и на платине под давлением ниже 1 мм рт, ст. является реакцией первого порядка и тормозится азотом и водородом. При давлении выше 1 мм рт. ст. тормозящее действие оказывает только водород. [1]
Разложение аммиака на железных катализаторах, активированных AlzOs iK O, является реакцией первого порядка, при давлении около 150 мм рт. ст. она превращается в реакцию нулевого порядка. Реакция тормозится водородом, степень уменьшения скорости разложения зависит от температуры. [2]
Разложение аммиака на водород и азот производится не только при накаливании и действии электрических искр, но также посредством многих окисляющих веществ, напр. Воду, при этом происходящую, можно взвесить, а количество азота можно измерить в газообразном виде и таким образом определить состав аммиака; этим способом получают, что в аммиаке на 14 вес. По объемам же аммиак состоит из 3 объемов водорода и 1 объема азота, образующих 2 объема аммиака. [3]
Разложение аммиака на его элементы при нагревании в контакте с другими материалами было замечено еще в XIX столетии, причем наблюдалось также влияние железа на реакцию. В 1884 г. Рамзай и Юнг ( Ramsay и Young) опубликовали свою работу относительно скорости разложения аммиака при различных условиях и снова отметили каталитическое действие железа на реакцию. Помимо всего прочего Рамзай и Юнг установили, что даже если пропускать аммиак медленно через железную трубу, доведенную до красного каления, все же следы аммиака остаются не разложившимися; в конце своей работы они сделали следующее многозначительное замечание: На основании этого результата, а также и на основании наблюдения Девиля ( Deville), что разложение аммиака никогда не бывает полным при пропускании искры, становится очевидным, что должно иметь место обратное соединение азота и водорода, хотя бы в самых незначительных размерах. Принимая во внимание это утверждение, является весьма любопытным тот факт, что целый ряд более поздних исследователей цитирует Рам-зая и Юнга в доказательство того, что реакция разложения аммиака необратима. [4]
Разложение аммиака на поверхности вольфрама происходит при относительно высоких температурах. [5]
Разложение аммиака начинается при 270 С, а при температуре свыше 900 С аммиак практически разлагается полностью. [6]
Разложение аммиака до азота и водорода обычно протекает с образованием промежуточных частиц. [7]
Разложение аммиака, пиридиновых оснований и фенолов увеличивается при недостаточной загрузке коксовой камеры угольной шихты. При этом время пребывания химических продуктов в зоне высоких температур увеличивается, а следовательно, растет и степень разложения этих продуктов. [8]
Разложение аммиака на платине сильно тормозится водородом ( ср. [9]
Разложение аммиака на азот и водород может происходить при высокой температуре на пути подвода аммиачно-кислород-ной смеси к контактному аппарату и катализатору, а разложение окиси азота на азот и кислород возможно после прохождения катализатора и на выходе из контактного аппарата. [10]
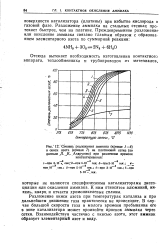 |
Степень разложения аммиака ( кривые 1 - 6. [11] |
Разложение аммиака на стальных стенках протекает быстрее, чем на платине. [12]
Разложение аммиака на таких металлах, как вольфрам, платина и молибден при низких давлениях ( менее 1 атм), изучалось довольно часто. При температурах вблизи 1000 наблюдается слабая хемосорбция и скорость-определяющей стадией, по-видимому, уже является какая-то из поверхностных стадий, а не десорбция азота; вероятно, эти стадии имеют низкую энергию активации ( по данным реакций обмена - 13 - 20 ккал / моль) и их скорости не возрастают одновременно с десорбцией при повышении температуры. [14]
Разложение аммиака часто применяется для изучения механизма обратной ей важной промышленной реакции синтеза аммиака на металлах. Возникает вопрос, сохраняются ли особые свойства конфигурации с. Фосфиды и нитриды переходных металлов, на которых изучалось разложение NH3 [432, 433], также имеют металлическую проводимость. На d - уровнях металла в них обычно находится больше электронов, чем в чистом металле. Параметры решеток этих веществ ( см. Приложение) довольно близки друг к другу. [15]
Страницы: 1 2 3 4