Разложение - метанол
Cтраница 1
Разложение метанола на высокодисперсном цинке, адсорбированном на силикагеле и на цинке в кристалле полупроводника ( катализаторы ZnS Си с содержанием меди меньше 10 - 5 г / г), судя по составу образующегося газа, идет в одном направлении, но энергия активации процесса для цинка на силикагеле понижается до 20 ккал. Таким образом, каталитические свойства атома, частично внедренного в кристаллическую решетку полупроводника, лишь незначительно изменяются при вынесении его на поверхность инертного носителя. [1]
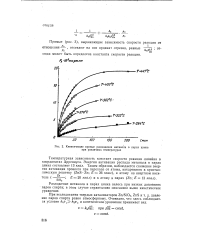 |
Кинетические кривые разложения метанола в парах цинка при различных температурах. [2] |
Разложение метанола в парах цинка велось при низких давлениях паров спирта; в этом случае справедливо описанное выше кинетическое уравнение. [3]
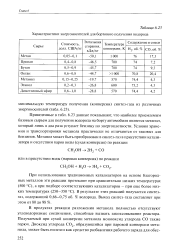 |
Характеристики энергоносителей для бортового получения водорода. [4] |
В продуктах реакции разложения метанола полностью отсутствуют углеводородные соединения, способные вызвать закоксовывание реактора. Получаемый при сухой конверсии метанола монооксид углерода СО также горюч. [5]
По отношению к реакции разложения метанола при 328 удельная активность дымовых препаратов превосходит активность пиролитических контактов. Различие вторичных структур этих препаратов влечет за собой резко отличное поведение их при нагревании. [6]
Золотев и Шапиро [409], изучая разложение метанола на медно-цинковом катализаторе, полагали, что избирательная активность катализатора зависит от его структуры. [7]
Хромит цинка является классическим катализатором синтеза и разложения метанола. Использование этого катализатора в процессах разложения метанола до СО и Н2 при небольших масштабах производства оправдывает затраты на сырье. [8]
Обсуждается так называемая экономичная водородно-топ-ливная система, использующая разложение метанола на водород и оксид углерода ( последний является источником водорода по реакции СО Н2О), в результате чего из удобного для хранения и транспортировки жидкого метанола в очень мягких условиях получается поток водорода. Такой процесс вполне возможно реализовать в автомобилях или в жилых домах. [9]
В работе Ло и Франсуа [9] содержится краткое упоминание о разложении метанола, адсорбированного на нитевидных образцах Ge при прокаливании последних. [10]
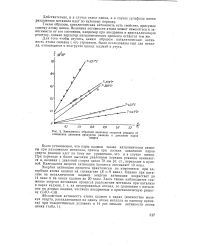 |
Зависимость обратной величины скорости реакции от отношения давления продуктов реакции к давлению паров. [11] |
Было установлено, что пары кадмия также каталитически активны при разложении метанола, причем при низких давлениях паров спирта реакция идет по тому же уравнению, что и в случае цинка. При переходе к более высоким давлениям порядок реакции изменяется и, начиная с давлений спирта около 70 мм рт. ст., переходит в нулевой. Кажущаяся энергия активации процесса составляет 10 ккал. [12]
Иод довольно часто применяется при парофазном ( 300 - 550 С) гомогенно-каталитическом разложении метанола [45], альдегидов [37-39, 43], кетонов [36] и многих эфиров [39- 43, 45]; е результате этих процессов образуются окись углерода, парафины, олефины, водород. [13]
Действительно, и в случае окиси цинка, и в случае сульфида цинка разложение метанола идет по нулевому порядку. [14]
Пшежецкий [ Ii04 ] также обнаружили уменьшение начальной каталитической активности ZnO для реакции разложения метанола после воздействия у-излуче-ния в атмосфере кислорода. [15]
Страницы: 1 2 3 4