Разложение - селитра
Cтраница 2
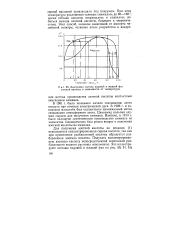 |
Диаграмма состава паровой и жидкой фаз азотной кислоты в зависимости от температуры. [16] |
При этом температура разложения селитры снижалась до 80 - 160Э, время отгонки кислоты сокращалось и удавалось добиться выхода азотной кислоты, близкого к теоретическому. [17]
Часть веществ оказывает замедляюшее действие на разложение селитры только при высоком содержании их в смеси. К ним относятся многие растворимые в воде соли. Имеются и нейтральные по своему действию примеси, не изменяющие скорость разложения, например железо, олово, аммоний [ 9, с. Сюда же относятся кварц, полисиликаты и ряд других нерастворимых в воде и практически не взаимодействующих с азотной кислотой и двуокисью азота веществ. Показано [44], что NO2 и азотная кислота катализируют разложение. Поэтому введение в селитру связывающих эти соединения примесей стабилизирует ее. [18]
Это способ В а-лентинера, при котором разложение селитры серной кислотой производят при пониженном давлении, вследствие чего реакция происходит при более низкой температуре ( 120 - 130), чем при нормальном давлении. Благодари низкой температуре реакции азотная кислота не разлагается, и получается продукт, не содержащий окислов азота. Кроме того процесс при этих условиях ускоряется. [19]
В производстве аммиачной селитры большую опасность представляет возможность разложения селитры, протекающего со взрывом. Сухая селитра взрывается от детонатора. Заметное термическое разложение ее начинается при температуре выше 200 С. В присутствии некоторых примесей ( свободные кислоты, хлориды, органические вещества) температура разложения селитры снижается. [20]
Как показала эксплуатация опытного аппарата в Невинно-мнсске, контроль за степенью разложения селитры в аппарате по содержанию закиси азота в выходящей из аппарата воздухе крайне неоперативен ( длителен и сложен) и может применяться только как разовый контрольный анализ, подгвер - кдающий тот факт, что при установленной норне кислотности плава на выходе из аппарата закись азота в выхлопных газах обнаруживается в ничтожных количествах. Проще о степени разложения ыожно судитъ-по кислотности плава на выходе из аппарата. [21]
Причина хода реакции в этом случае та же, как при разложении селитры серною кислотою; только там получается гидрат, а здесь ангидрид кислоты, потому что гидрат углекислоты Н2СО3 непостоянен и тотчас, как выделяется, разлагается на воду и свой ангидрид. Очевидно, из объяснений причины действия серной кислоты на селитру, что не все кислоты могут служить для получения углекислого газа; именно, те не будут выделять его, которые или очень, химически, мало энергичны, или в воде нерастворимы, или сами столь же легко летучи, как угольная кислота. [22]
Кроме влияния на концентрацию дефектов в кристаллической решетке, примеси могут изменять температуру разложения селитры в ту или иную сторону. Надо сказать, что в целом механизм влияния определяется не только химическими свойствами добавки, но и степенью соответствия параметров кристаллических решеток добавок и азотнокислого аммония. Соотношение этих параметров, наряду с другими факторами, определяет возможность образования твердых растворов, а следовательно, и степень влияния. Разумеется, сказанное справедливо в тех случаях, когда в основе механизма действия примеси на кинетику разложения лежит растворение одного вещества в другом в твердом состоянии. [23]
При получении аммиачной селитры он вводится в азотную кислоту, нейтрализуемую затем аммиаком. Скорость разложения селитры, в частности, может определяться весовым методом. Исследования показали, что при содержании в селитре не менее 0 2 - 0 3 о карбамида происходит значительное торможение процесса ее распада. Интересно отметить, что действие карбамида проявляется достаточно ярко и в присутствии таких ускорителей разложения, как смазочные масла и хлориды металлов. Карбамид сохраняет свою эффективность в аммиачной селитре различных сортов, в том числе и в водоустойчивой селитре, идущей на изготовление взрывчатых веществ. [24]
С увеличением температуры разложение селитры значительно ускоряется. [25]
В производственных условиях наибольшую опасность представляет возможность взрывчатого разложения и детонации концентрированных растворов и плава аммиачной селитры. При этом вероятность разложения селитры возрастает с повышением температуры. Поэтому Правилами и нормами техники безопасности производства аммиачной селитры, изданными в 1962 г., предельная их температура в аппаратуре ограничивается значением 170 С. В последние годы в связи с интенсификацией процессов нейтрализации и получения селитры предельная температура нагрева растворов ( плава) установлена 190 С. [26]
Получается дымящая кислота разложением селитры серной кислотой при энергичном нагревании. Какие изменения происходят при этом с азотной кислотой и каков состав газов, окрашивающих ее, вы узнаете из следующих работ. [27]
При нагревании аммиачная селитра теряет аммиак. При температуре выше 200 разложение селитры ускоряется, выделяется кислород, и она становится взрывчатой и огнеопасной. Взрывчатые свойства аммиачной селитры проявляются при неблагоприятных условиях ее хранения. Следует также иметь в виду, что при хранении аммиачной селитры могут происходить превращения одной кристаллической формы в другую ( перекристаллизация); это также способствует слеживаемости. [28]
При нагревании аммиачная селитра теряет аммиак. При температуре выше 200 разложение селитры ускоряется, выделяется кислород, и она становится взрывчатой и огнеопасной. [29]
Термическое разложение аммиачной селитры значительно ускоряется в присутствии азотной, серной, сшяной кислот. В присутствии кислоты снижается температура начала разложения селитры. При повышении содержания свободнрй кислоты до 1 % температура начала активного разложения селитры снижается с 210 до 185 - 190 С. Каталитическое действие на термическое разложение селитры оказывают примеси хлоридов, хроматов, соединения кобальта. [30]
Страницы: 1 2 3