Разложение - гидроперекись
Cтраница 1
Разложение гидроперекисей, образующихся у третичных углеродных атомов, приводит к распаду углерод-углеродной связи, как показано в реакции ( XII1 - 10), где R - ответвление от основной цепи. [1]
Разложение гидроперекиси обычно ведут непрерывным методом, раздельно подавая концентрат гидроперекиси и кислотный катализатор ( обычно серную кислоту) в аппарат или каскад аппаратов с продуктами разложения гидроперекиси и собирая вытекающий раствор в приемник. Температуру поддерживают приблизительно при 50 - 90 С, причем значительное тепловыделение ( 226 кДж / моль) снимается с помощью охлаждающих змеевиков или за счет испарения ацетона. [2]
Разложение гидроперекисей, катализируемое солями металлов переменной валентности, протекает по сложному механизму с участием ионов и свободных радикалов. [3]
Разложение гидроперекиси проводят в реакторе 11 с поперечными перегородками. Из последней секции реактора / / продукты непрерывно выводят на разделение после предварительной нейтрализации серной кислоты водным раствором щелочи. Схема разделения реакционной массы на фенол и ацетон обычна и не представляет определенного интереса, поэтому на схеме не показана. Наиболее опасны процессы окисления изопропилбензола, ректификации и дистилляции гидроперекиси и разложения гидроперекиси изопропилбензола. [4]
Разложение гидроперекиси проводят в реакторе 11 с поперечными перегородками. Из последней секции реактора 11 продукты непрерывно выводят на разделение после предварительной нейтрализации серной кислоты водным раствором щелочи. Схема разделения реакционной массы на фенол и ацетон обычна и не представляет определенного интереса, поэтому на схеме не показана. Наиболее опасны процессы окисления изопропилбензола, ректификации и дистилляции гидроперекиси и разложения гидроперекиси изопропилбензола. [5]
Разложение гидроперекисей происходит в присутствии оснований. [6]
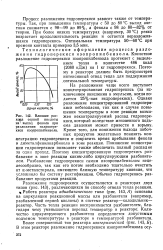 |
Влияние расхода серной кислоты на выход фенола при разложении гидроперекиси изопропилбензола. [7] |
Разложение гидроперекиси осуществляется в реакторах двух типов ( рис. 143), различающихся по способу отвода тепла реакции. Работа реактора адиабатического типа ( рис. 143, Л) основана на циркуляции реакционной массы или разбавителя ( например, разбавленной серной кислоты) в системе реактор-холодильник - реактор. Количество циркулирующего разбавителя определяется допустимым подъемом температуры в реакторе и температурой разбавителя. [8]
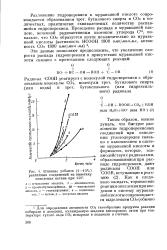 |
Влияние добавок ( 4 - 10 %. [9] |
Разложение гидроперекиси в муравьиной кислоте сопровождается образованием трет, бутилового спирта и ССЬ в количествах, практически эквивалентных количеству распавшейся гидроперекиси. Проведение распада в муравьиной кислоте, меченной радиоактивным изотопом углерода С14, показало, что GO2 образуется почти исключительно из муравьиной кислоты ( активность НСООН 1800 имп / мин. [10]
 |
Термический распад гидроперекиси emop - бутил-бензола в зависимости от температуры. [11] |
Разложение гидроперекиси ewop - бутилбензола на метилэтилкетон и фенол. [12]
Разложение гидроперекиси ( вторая реакция) проводят под давлением кипячением с разбавленной серной кислотой. Этот метод является наиболее перспективным, поскольку одновременно с фенолом получают ценный продукт - ацетон. В промышленном масштабе впервые он был осуществлен в СССР в 1949 г. Сырье для данного метода доступно и дешево. Выход фенола из изопропилбензола составляет около 93 % от теоретического. [13]
Разложение гидроперекиси с образованием свободных радикалов, ведущих к вырожденному разветвлению, определяет в основном скорость реакции по окончании индукционного периода окисления масла. Деактивация - разложение гидроперекисей - не только удлиняет индукционный период, но и уменьшает скорость развившейся реакции. [14]
Разложение гидроперекиси в присутствии кадмий-бариевого катализатора с различным содержанием ее в оксидате при температуре 120 иллюстрирует рисунок. Как видно, разложение гидроперекиси с концентрацией 1 моль / л в оксидате в течение 20 часов не происходит. [15]
Страницы: 1 2 3 4