Разложение - гидроперекись
Cтраница 2
Разложение гидроперекиси определяет автокаталитическое развитие процесса окисления и приводит к образованию наблюдаемых нами альдегидных, сложноэфирных и кислотных групп. Количественное соотношение этих групп, возможно, определяется различной вероятностью разрыва связей в пе-рекисном радикале I. При этом преобладает процесс образования альдегидных групп. Радикалы II, III, IV продолжают цепь окисления или рекомбинируют. [16]
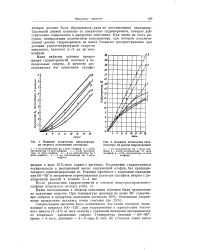 |
Влияние количества катализатора [ IMAGE ] Влияние количества ката. [17] |
Разложение гидроперекиси осуществляли в реакционной массе, содержащей олефин, без предварительного концентрирования ее. Реакция протекает с хорошими выходами при 60 - 65 и энергичном перемешивании раствора сульфита натрия с реакционной массой в течение 3 - 4 час. [18]
Разложение гидроперекиси в принципе можно вести без концентрирования ( кроме производства двухатомных фенолов, когда необходимо предварительное разделение моногидроперекиси и ди-гидроперекиси); в этом случае фенолы можно было бы выделить ректификацией или экстракцией щелочью непосредственно из реакционной массы. Однако разложение гидроперекиси в присутствии большого избытка непрореагировавшего углеводорода неизбежно привело бы к образованию продуктов взаимодействия с углеводородом и в конечном счете к большим потерям гидроперекиси и увеличению выхода побочных продуктов. Сложно и связано со значительными потерями выделение фенола из такой бедной смеси. [19]
Разложение гидроперекиси в этой реакции, вероятно, происходит за счет сиккатива. Присутствием сиккатива, по-видимому, обусловливается также и поглощение кислорода. Возможно также дальнейшее взаимодействие между сопряженными двойными связями ( схема 5в) и простой двойной связью ( схема 5а), хотя этот процесс обычно имеет место при термической полимеризации. Однако возможно, что связывание кислорода сиккативами ( схема 5 ( 5) может каталитически ускорить эту реакцию, и последняя будет происходить при нормальной температуре. Это явление подтверждается тем, что пленки масел при высыхании на воздухе в присутствии сиккативов содержат меньше кислорода, чем в случае воздушной сушки без сиккативов. Этим можно также объяснить низкое содержание кислорода в пленках масел с сопряженными связями и их способность быстро высыхать. [20]
Разложение гидроперекиси изопропилбензола в смеси изопропилового спирта с бензолом приводит к образованию ацетона, диметилфенил-карбинола, ацетофенона и а-метилстирола. Скорость этой реакции зависит от состава растворителя, концентрации гидроперекиси и температуры. [21]
Разложение гидроперекиси изопропилбензола в смеси изопро-гшлового спирта с бензолом приводит к образованию ацетона, ди-метплфенилкарбинола, ацетофенона и а-метилстирола. Скорость, этой реакции зависит от состава растворителя, концентрации гидроперекиси и температуры. [22]
Разложение концентриропанной гидроперекиси следует проводить весьма осторожно, не допуская бурного протекания реакции, которая может перейти по взрып. При разложении необходимо интенсивно отводить тепло реакции и избегать применения концентрированной серной кислоты. Аппарат заполняют смесью фенола и ацетона и плодят в пего гидроперекись. Для разложения применяют 1с / 0-ный раствор серной кислоты п феноло-ацетоновой смеси. Тепло реакции отподят п выносном холодильнике 21, имеющем большую поверхность теплообмена, что позво лист поддерживать п аппарате 19 температуру 40 - 60 С. [23]
Разложение гидроперекисей вторичных алкилов может протекать различно, в зависимости от условий. [24]
Разложением гидроперекиси изопропилбензола получают фенол и ацетон. [25]
Для разложения гидроперекиси применяют 1 % - ный раствор серной кислоты в фенолацетоновой смеси. [26]
Для разложения гидроперекиси могут применяться различные кислоты; на практике применяют серную кислоту. Концентрация кислоты оказывает значительное влияние на скорость превращения гидроперекиси. Например, с 10 % - ным раствором серной кислоты это превращение может окончиться за 1 час, тогда как при концентрации кислоты в 1 % требуется 5 час. При применении концентрированной серной кислоты на превращение требуется менее 1 мин. [27]
Проведено разложение гидроперекиси rper - бутила в окисляющемся изопентане, На основании состава продуктов, образующихся при разложении гидроперекиси-трет-бутшш и окислении изопептаиа, сделано предположение о том, что при рекомбинации пероксирадикалов, главным образом, получаются алкоксирадикалы, кото-рье ведут цепь окисления, взаимодействуя с гидроперекисью, что приводит к уско-репному ее разложению в условиях окисления. [28]
Проведено разложение гидроперекиси грег-бутила в окисляющемся изопентане. На основании состава продуктов, образующихся при разложении гидроперекиси трет-бутила и окислении изопентана, сделано предположение о том, что при рекомбинации пероксирадикалов, главным образом, получаются алкоксирадикалы, кото-рь. [29]
Для разложения гидроперекисей к окисленному продукту при температуре 20 - 30 С прибавляли 10 % - ный раствор NaOH ( 20 % от веса оксидата), затем смесь нагревали до 75 - 80 С и перемешивали при этой температуре в течение 15 - 20 мин. [30]
Страницы: 1 2 3 4