Гомогенное разложение
Cтраница 3
Изменение скорости гомогенного и гетерогенного разложения перекиси водорода в зависимости от состава сплавов симбатно изменению их коорозионной стойкости ( ср. Связь между скоростью гомогенного разложения и коррозионной стойкостью обусловлена переходом в раствор каталитически активных ионов меди. [32]
Работы же, цитированные ниже, показывают, что введение электроиодонорпых заместителей в перекиси ацилов ускоряет разложения. Так, если рассматривать гомогенное разложение в газовой фазе, то органические перекиси, по-видимому, менее устойчивы, чем перекись водорода. Наоборот, пример реакций с ионом закисного железа показывает, что перекись водорода является наиболее реакционноспособпой из всех изученных перекисей. В частности, нужно различать чувствительность какой-либо перекиси к взрыву или детонации и скорость, с которой она подвергается реакции в строго определенных УСЛОВИЯХ. [33]
Скорость адсорбции не меняется с температурой каталитической поверхности, и теплота активации, вычисленная из температурного коэффициента, оказалась равной 25 000 кал на моль. С другой стороны, гомогенное разложение йодистого водорода имеет теплоту активации 44 000 кал. Этот результат привел исследователей к заключению, что теплоты активации соответствующих гетерогенных и гомогенных реакций находятся приблизительно в отношении 1: 2 и что в то время как гомогенная реакция бимолекулярна, гетерогенная реакция - мономолекулярна. Шпитальский и Каган [527] применили принципы электронной поляризации для объяснения механизма гетерогенного катализа. Недавно [24, 25] разработана теория дегидрогениза-циоиного катализа. Она интерпретирует гетерогенные каталитические реакции с точки зрения мультиплетной гипотезы, в основе которой лежит утверждение, что связь между атомами разрывается, если они притягиваются двумя различными атомами катализатора. Согласно этой гипотезы катализ является следствием геометрически определенного действия различных каталитических центров. Кроме того, исследованиями [26] дегидрогенизации циклогексана и спирта в присутствии палладия, подвергаемого ультрафиолетовой радиации ртутной лампьш не подвергаемого о блучению, было установлено, что о блучение каталитической поверхности ультрафиолетовойрадиацией, кванты которой больше, чем кванты, соответствующие теплоте активации каталитической реакции, не вызывает ускорения реакции. Неактивный катализатор также не становится активным под действием радиации. Свойства свободной поверхности и скорость перехода энергии в соответствующих случаях гетерогенного катализа объясняют получающийся эффект. Квантово-механическое объяснение гетерогенного катализа, даваемое Франком [167], допускает, что каталитический процесс происходит путем превращений, у которых теплота активации не превышает потенциального порога, но при этом пронизывается потенциальный барьер. Франк считает, что в этом процессе вероятности превращения благоприятствуют близость молекул в адсорбированном состоянии и выравнивание потенциальных стенок. [34]
Радикалы, например гидроксил или пергидроксил, по-видимому, играют значительную1 роль в процессах разложения перекиси водорода, но в связи с образованием их в качестве промежуточных продуктов рассматривать эту роль целесообразнее при дальнейшем анализе разложения в присутствии отдельных элементов. Лучше всего вопрос о значении этих частиц разработан при исследовании гомогенного разложения в присутствии железа. [35]
Можно видеть, что концентрация перекиси водорода проходит через максимум. Падение концентрации перекиси водорода при увеличении времени реакции может быть вызвано гетерогенным разложением ее на стенках реактора, гомогенным разложением или реакциями в газовой фазе с другими присутствующими химическими частицами. Количества выделенной перекиси водорода сильно колеблются в зависимости от характера поверхности реактора. [36]
ПАН-1 и ПАН-2 оказывают также каталитическое действие на реакцию разложения гидразин-гидрата в направлении образования аммиака и азота. Однако заметное каталитическое разложение гидразин-гидрата имеет место при сравнительно высоких температурах ( 250), при которых существенную роль играет реакция на стеклянной поверхности реактора и гомогенное разложение. [37]
ПАН-i и ПАН-2 оказывают также каталитическое действие на реакцию разложения гидразингидрата в направлении образования аммиака и азота. Однако заметное каталитическое разложение гидразингидрата имеет место в условиях сравнительно высоких температур ( 250 С), при которых существенную роль играет реакция на стеклянной поверхности реактора и гомогенное разложение. [38]
Первой стадией процесса выделения фенола и ацетона из этой смеси является нейтрализация кислот более сильных, чем фенол. Методы дальнейшей очистки бывают различными и зависят от того, проводилось ли разложение гидроперекиси в гетерогенной или гомогенной среде. Шервуд указывает, что при гомогенном разложении во время последующей нейтрализации образуется небольшой водный слой, в котором содержание фенола и ацетона сравнительно невелико. В процессе нейтрализации, особенно при гомогенном процессе, осаждается сульфат натрия, что вызывает небходимость фильтрации смеси. [39]
Пожалуй, наименее резко изменяется характер растворителя при замещении части или всей воды, применяемой в качестве растворителя, тяжелой водой; правда, этот метод имеет то неудобство, что при его применении одновременно изменяются и растворитель и растворенное вещество, так как перекись водорода быстро обменивается водородом с растворителем. Такого рода исследования показали, что гетерогенное разложение под действием платины 1132, 133 ], стекла и золота [134] в присутствии тяжелой воды замедляется. В двух сообщениях [135, 136] утверждается, что в этих условиях гомогенное разложение йодидом также замедляется, однако в третьей работе [133] влияние тяжелой воды на реакцию не обнаружено. [40]
Исследования газофазного разложения перекиси водорода при 467 - 542, выполненныеМак - Лейном [11], показывают, что по меньшей мере в некоторой части разложение является гомогенным. Результаты работ этого автора приводят к энергии активации от 40 до 50 ккал / моль. Логично предполагать, что только при таких высоких температурах может иметь место термически активированное гомогенное разложение перекиси водорода с измеримой скоростью. Это подчеркивает также Харт [12], который приходит к следующему заключению. [41]
Удержание, наблюдаемое в некоторых реакциях разложения твердых веществ, представляет собой явление в высшей степени индивидуальное по своему характеру, а потому оно будет рассмотрено в разделах, посвященных описанию кинетики отдельных реакций. Однако следует все же рассмотреть связанную с этим проблему окклюзии газа. Она обсуждалась недавно Гафнером - 171 ], который рассмотрел диффузионное удаление газа, образующегося внутри частиц, подвергающихся гомогенному разложению. Это крайне маловероятный случай, возможен он только в самых неблагоприятных условиях, которые можно себе представить. Если радиус частиц равен 10 - 3 см, а величина константы скорости составляет около 10 - 3 сек 1, то в пределах возможных экспериментальных ошибок не будет наблюдаться различий при изменении коэффициента диффузии от 10 - 9 см - сек-1 до бесконечности. Такое понижение скорости достаточно велико, чтобы объяснить удержание спеканием продукта. [42]
Гомогенный катализ разложения перекиси водорода в присутствии железа изучен очень подробно и глубоко. В связи с этим имеется довольно подробное описание этого процесса, хотя на многие вопросы еще не получено ответа. Ниже рассматриваются следующие аспекты этого катализа: разложение перекиси водорода с одновременным окислением иона закисного железа в окисное, механизм гомогенного разложения, вызываемого ионом трехвалентного железа, торможение и усиление этого катализа, разложение под действием железа в комплексной форме и гетерогенный катализ на железе. [43]
Расщепление метана может происходить в свободном объеме-гомогенно или на насадке ( катализаторе) - гетерогенно. Гомогенное разложение метана характеризуется образованием тонкодисперсного углерода, уносимого газовым потоком из зоны реакции. При гетерогенном распаде метана на поверхности контакта отлагается плотный слой углерода: Экспериментально показано [101], что температура гетерогенного разложения метана может быть на 150 - 200 С ниже, чем гомогенного разложения. [44]
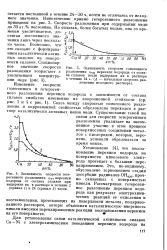
Так, гомогенное разложение ряда перекисей, например диэтилперекиси, дибензоилперекиси и ди-трет-бутилперекиси, гидроперекиси кумола и пероксосульфата, протекающее с гемолитическим разрывом связи О-О в газовой или жидкой фазе, обладает энергиями активации около 30 - 40 ккал / моль. Энергии активации при реакциях с другими веществами лежат ниже этого интервала и составляют всего лишь 10 ккал / моль. Как показывают приведенные на рисунке данные, для этой частной реакции между предэкспоненциальным множителем и энергией активации имеется прямая пропорциональность. При заданной температуре это соотношение показывает, что все приведенные на рисунке заместители в перекиси водорода снижают скорость реакции. В данном случае положение как раз обратно наблюдаемому при некаталитическом гомогенном разложении органических перекисей, где другие перекиси разлагаются быстрее, чем перекись водорода. Орр и Вильяме [ 14] интерпретируют результаты реакции с ионом закисного железа ( рис. 57) таким образом, что отталкивание избыточного электрона в связь О-О снижает энергию активации за счет увеличения числа электронов, способных к координации с закисным железом в активированном комплексе. [45]
Страницы: 1 2 3 4