Размер - противоион
Cтраница 1
Размер противоиона проявляется двояко: во-первых, по теории Грегора, он сказывается на селективности, что выражается в преимущественном поглощении смолой меньших ионов; во-вторых, при определенных размерах противоиона может быть достигнута крайняя форма того же явления, а именно ионного сита. [2]
Кроме того, как и при обмене одновалентных катионов, кинетические параметры обмена одно-двухвалентных катионов также возрастают с уменьшением размера противоиона. Подвижность щелочноземельных катионов в клиноптилолите убывает в ряду Са Sr Ba, который также указывает на увеличение скорости обмена с уменьшением размера противоиона и является обратным по отношению к ряду селективности. [3]
Крупные низкозаряженные катионы и анионы типа ( CeHsbAs 1, ( СбН6) 4Р, С10Г, ReOr могут количественно экстрагироваться в присутствии больших по размеру противоионов с низким зарядом. Экстракцию ведут из кислой среды, в которой красители существуют в протонированной ( катион-ной) форме. Эффективными экстрагентами металлгалогенид-ных анионов, оксоанионов металлов, а также простых анионов являются высокомолекулярные амины, которые при экстракции из кислых растворов образуют в органической фазе соответствующие аммонийные соли. [4]
Набухание органических ионообменников является одним из наиболее важных свойств этих материалов, оно зависит главным образом от типа и свойств каркаса матрицы, величины обменной емкости, заряда и размера противоиона, типа связи между этим ионом и функциональными группами ионообменника, концентрации электролита в растворе и полярности растворителя. [5]
Кроме того, следует отметить, что для одной и той же концентрации раствора значения константы скорости внешне - и внутридиффузионного процессов, а также эффективного коэффициента диффузии возрастают с уменьшением размера противоиона. Подвижность щелочных катионов в клиноптилолите убывает в ряду Li К Cs. Этот ряд указывает на увеличение скорости обмена с уменьшением размера противоиона и является обратным по отношению к ряду селективности. [6]
При обмене Na - / 2 РЬ2 время достижения 50 % степени обмена ( г j / 2) и равновесия ( тх) оказалось значительно меньше, чем при обмене N а - / 2Sr2, хотя размеры противоиона близки между собой. [7]
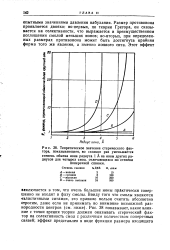
На рис. 5 и 6 приведены кривые, характеризующие влияние степени поперечной сшитости и числа зарядов противоионов, а также концентрации внешнего раствора на набухание ионитов. Набухание зависит также от размера противоиона. Про-тивоион, имеющий в гидратированном состоянии больший радиус, будет вызывать большее набухание. Например, катионит в Li-форме набухает значительно больше, чем в Cs-форме. Однако это правило соблюдается не всегда. [8]
Размеры полииона на несколько порядков превышают размеры противоионов. [9]
Причем в области низких концентраций противоиона в растворе эти цеолиты проявляют отчетливую селективность к катионам щелочноземельных металлов, при этом, как и для щелочных катионов, селективность убывает в ряду: клиноптилолит эрионит морденит. Между этими цеолитами существует значительное различие по избирательности в зависимости от размера противоиона. Для клиноптилолита характерна групповая селективность к катионам Ва2, Sr2 и Са2 со слабовыраженным различием в избирательности в зависимости от размера противоиона, а для морденита и эрионита селективность сильно зависит от радиуса входящего иона. [10]
Характерная черта этих цеолитов - их резко выраженная селективность к крупным катионам щелочных металлов, убывающая в ряду клиноптилолит - филлипсит - эрионит - морденит. Кроме того, эти цеолиты значительно различаются по избирательности в зависимости от размера противоиона. [11]
На первый взгляд, эти ряды являются бессистемными и не подтверждают найденной общей закономерности увеличения селективности с возрастанием размера противоиона. [12]
Кроме того, как и при обмене одновалентных катионов, кинетические параметры обмена одно-двухвалентных катионов также возрастают с уменьшением размера противоиона. Подвижность щелочноземельных катионов в клиноптилолите убывает в ряду Са Sr Ba, который также указывает на увеличение скорости обмена с уменьшением размера противоиона и является обратным по отношению к ряду селективности. [13]
На некоторых стадиях каталитической реакции могут реагировать одноименно заряженные частицы. Процессы такого типа из-за значительного электростатического отталкивания между частицами реагентов требуют значительной энергии активации, особенно в случае многозарядных частиц. В таких случаях введение в систему небольших по размерам противоионов может привести к существенному снижению энергии активации и благоприятствовать протеканию процесса. Для этого необязательно, чтобы про-тивоион включался в координационную сферу одного из реагентов. Активирующее действие такого типа может наблюдаться в реакциях, протекающих как по внутрисфер-ному, так и по внешнесферному механизму. Активатор здесь уменьшает энергетический барьер, препятствующий сближению реагентов. [14]
Кроме того, следует отметить, что для одной и той же концентрации раствора значения константы скорости внешне - и внутридиффузионного процессов, а также эффективного коэффициента диффузии возрастают с уменьшением размера противоиона. Подвижность щелочных катионов в клиноптилолите убывает в ряду Li К Cs. Этот ряд указывает на увеличение скорости обмена с уменьшением размера противоиона и является обратным по отношению к ряду селективности. [15]
Страницы: 1 2