Размешивание - электролит
Cтраница 2
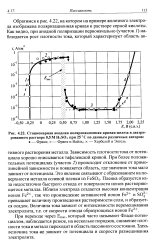 |
Стационарная анодная поляризационная кривая железа в деаэрированном растворе 0 5 М H2SO4 при 25 С по данным различных авторов. [16] |
При переходе через Епас который часто называют Фладе-потен-циалом, наблюдается резкое, на несколько порядков, снижение плотности тока и металл переходит в область пассивного состояния. Здесь величина тока-не зависит от потенциала и скорости размешивания электролита. [17]
Механическое перемешивание электролита вращающимся анодом особенно удобно при наращивании металла на поверхности монолитных форм, внутрь которых помещают анод. На рис. 44 показан станок, применяемый автором для размешивания электролита этим способом. Анод, перемешивая электролит, поворачивается своими плоскостями ко всем стенкам формы. Одновременно в форму насосом подается свежий электролит из дополнительной ванны, в которую отработанный электролит сифоном возвращается обратно на фильтр. [18]
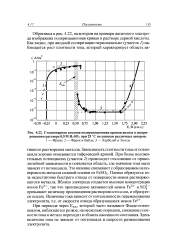 |
Стационарная анодная поляризационная кривая железа в деаэрированном растворе 0 5 М H2SO4 при 25 С по данным различных авторов. [19] |
При переходе через Епас, который часто называют Фладе-потен-циалом, наблюдается резкое, на несколько порядков, снижение плотности тока и металл переходит в область пассивного состояния. Здесь величина тока не зависит от потенциала и скорости размешивания электролита. [20]
Отрицательные значения двумерного давления ( я0) в этих условиях отражают растянутое состояние адсорбционных пленок. На жидких электродах при этом становятся возможными тангенциальные движения поверхности, приводящие к размешиванию электролита и вызывающие так называемые полярографические максимумы третьего рода ( см. гл. Для экспериментального определения адсорбционных параметров, входящих в изотерму Фрумкина, поступают следующим образом. Вначале на кривой зависимости ГА от lgcA графическим способом ищут центр симметрии: верхняя часть графика должна совмещаться с нижней его частью при повороте графика на 180 относительно центра симметрии. [22]
Разработанный Чутой и Кучерой [374, 375] метод определения йодных чисел ненасыщенных жирных кислот с одной двойной связью ( например, эруковой кислоты) основан на присоединении хлора, генерируемого из раствора НС1 в уксусной кислоте. В титрационную ячейку вводят 1 - 5 мл раствора эруковой кислоты в ледяной уксусной кислоте, прибавляют туда такое количество 100 % - ной СН3СООН и 37 % - ной НС1, чтобы электролит содержал 80 - 90 % уксусной и 4 % соляной кислоты, разбавляют до общего объема 25 мл и генерируют хлор при непрерывном размешивании электролита. Конечную точку определяют биамперометрически. [23]
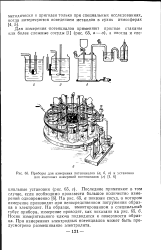 |
Приборы для измерения потенциалов ( а, б, б и установка для массовых измерений потенциалов ( г. [24] |
На рис. 65, а показан сосуд, в котором измерение производят при непосредственном погружении образца в электролит. Носик измерительного ключа подводится к поверхности образца. При измерениях электродных потенциалов может быть предусмотрено размешивание электролита. [25]
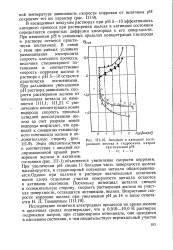 |
Анодная и катодная поляризация железа в гидроокиси натрия при значении рН. [26] |
В насыщенных воздухом растворах при рН 5 - 10 эффективность катодного процесса при растворении железа в активном состоянии определяется скоростью диффузии кислорода к его поверхности. При изменении рН в указанных пределах концентрация кислорода в растворе остается практи-чески постоянной. В связи с этим при равных условиях размешивания электролита скорость катодного процесса, величина стационарного потенциала и соответственно скорость коррозии железа в растворе с рН 5 - 10 остаются практически постоянными. [27]
Из этих кривых следует, что присоединение к катоду, работающему в условиях чисто диффузионного режима, любого анода, не выводящего потенциал системы за пределы величин, укладывающихся на вертикальной части кривой ( участок АВ), приводит к появлению одного и того же тока. Иными словами, ток подобных контактных пар определяется лишь величиной предельного диффузионного тока по кислороду и не зависит от природы и поляризуемости анода. Ток таких элементов должен сильно зависеть от интенсивности размешивания электролита ( ср. Когда же система приобретает потенциал, выходящий за пределы указанных выше границ, контактный ток должен зависеть как от скорости протекания самой электрохимической реакции, так и от скорости доставки деполяризатора к электроду и отвода продуктов анодной реакции. Степень влияния того или иного фактора, как будет показано ниже, зависит от скорости размешивания электролита. [28]
 |
Коэффициент диффузии и энергия активации восстановления Jli. [29] |
Для этой цели был выбран медный амальгамированный электрод в форме диска, диаметр которого, равный 54 0 002 мм, измерялся горизонтальным микроскопом. Условия эксперимента были выбраны так, что образующиеся после разряда атомы металлов полностью растворялись в амальгаме, и на поверхности электрода не происходило образование осадков. Было обращено особое внимание на то, чтобы соблюдался ламинарный режим размешивания электролита. [30]
Страницы: 1 2 3