Разновидность - атом
Cтраница 2
Изобарами называются разновидности атомов, имеющие одно и то же массовое число, но различные порядковые номера, следовательно, различные электронные оболочки. [16]
Изотопами называют разновидности атомов одного и того же элемента, отличающиеся между собой массой атомов ( атомным весом), но не отличающиеся зарядом ядра, количеством электронов и структурой электронных оболочек. [17]
Изотопами называют разновидности атомов одного и того же элемента, имеющие различные массовые числа, но одинаковый заряд ядра. [18]
Изотопами называются разновидности атомов данного элемента, которые обладают различными атомными весами, но одними и теми же химическими свойствами. [19]
ИЗОТОПЫ - разновидности атомов химического элемента, электрический заряд ядра которых одинаков, а масса различна. [20]
У каждой химической разновидности атомов возможно существование нескольких изотопов, отличающихся друг от друга числом нейтронов в ядре. [21]
Установлено существование разновидностей атомов химических элементов, ядра которых при одном и том же заряде обладают различной массой. Такие разновидности атомов названы изотопами. Изотопы - разновидности атомов химического элемента с одинаковым числом протонов, но с различным числом нейтронов в ядре; следовательно, у них одинаковое число электронов в оболочке и они занимают одно и то же место в периодической системе элементов. [22]
Все 272 отличные друг от друга разновидности атомов мы в первую очередь делим на 92 плеяды. [23]
Большая часть химических элементов имеет несколько разновидностей атомов, отличающихся друг от друга числом нейтронов N в ядре. К настоящему времени известно около 300 устойчивых и свыше 1000 неустойчивых изотопов. [24]
Согласно протонно-нейтронной теории ядер, изотопами называют разновидности атомов с одинаковым числом протонов и различным числом нейтронов в ядрах; изобарами - разновидности атомов с различным числом протонов и нейтронов, но одинаковым числом нуклонов. Такие атомы следовало бы, по предложению С. А. Щукарева, называть изонуклонами, так как при одинаковом массовом числе истинные массы двух изобаров не равны друг другу. [25]
Большинство элементов состоит из нескольких изотопов - разновидностей атомов с одним и тем же порядковым номером, но разными атомными весами. [26]
 |
Диаграмма монокристаллической серебряной пленки, полученная сканированием в электронном дифрактомстре. [27] |
Интересным в применении систем ДЭНЭ является возможность идентификации разновидности атомов, находящихся у поверхности путем анализа энергии вторичных электронов, эмиттированных во время наблюдения ДЭНЭ. [28]
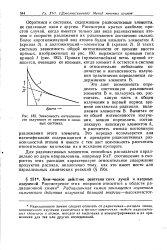 |
Зависимость интенсивно - из общей интенсивности излуче-сти излучения от времени в слож - ния, можно определить составных системах. ляющую вносимую элементом А, и рассчитать отсюда постоянную. [29] |
Это нередко используется для идентификации содержащихся в препарате радиоактивных разновидностей атомов и вместе с тем дает возможность рассчитать относительные количества их в исходном препарате. [30]
Страницы: 1 2 3 4