Разновидность - атом
Cтраница 3
Первые экспериментальные данные о существовании изотопов, как разновидностей атомов данного химического элемента, различающихся по массе ядер, были получены в 1906 - 1910 гг. при изучении свойств радиоактивных элементов. Содди был предложен и сам термин изотоп. Отметим, что под термином изотоп подразумевают и ядра таких атомов. Только изотопы водорода, в отличие от всех остальных, имеют собственные названия. Под символом Н в ядерной физике часто понимают только изотоп водорода Н, получивший название протий. Отметим, что нуклиды, содержащие одинаковое число нуклонов ( протонов и нейтронов) называются изобарами, а содержащие одинаковое число нейтронов - изотопами. [31]
Далее в ионе Н 2 связь между двумя разновидностями атома водорода - Ни р - возникает в симметричном состоянии относительно перестановки Н - р за счет обмена виртуальными электроном, обладающим мнимым импульсом. [32]
Но фосфор, встречающийся в природе, имеет только одну разновидность атомов - фосфор-31 ( 15 протонов плюс 16 нейтронов), следовательно, фосфор-30 - искусственный изотоп. Причина, по которой этот изотоп не встречается в природе, очевидна: период полураспада фосфора-31 составляет всего 14 дней. Излучение именно этого изотопа и наблюдали супруги Жолио-Кюри. [33]
Еще в 1881 г. А. М. Бутлеров предположил, что могут существовать разновидности атомов одного и того же элемента, обладающие одинаковыми химическими свойствами, но различные по массе. [34]
 |
Периоды полураспада некоторых изотопов. [35] |
Все элементы имеют, кроме стабильных изотопов, также и неустойчивые, радиоактивные разновидности атомов; большинство из них приходится, однако, приготовлять искусственно, так как в естественном состоянии на земле их нет или они так редки, что обнаружить их не удается. [36]
Не входя в рассмотрение отдельных реакций, в которых получаются эти разновидности атомов, отметим лишь, что многие из них могут получаться несколькими различными путями. [37]
В настоящее время найдено в природе и искусственно синтезировано свыше 1000 разновидностей атомов химических элементов, в том числе более 800 радиоактивных. [38]
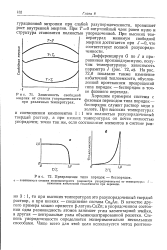 |
Зависимость свободной.| Превращение типа порядок - беспорядок. [39] |
В качестве другого примера можно привести р-латунь CuZn; в упорядоченном состоянии одна разновидность атомов занимает углы элементарной ячейки, а другая - центральные узлы объемноцентрированной решетки. Степень упорядоченности определяется экспериментально несколькими способами. [40]
Характеризуя представления Крукса, нужно обратить внимание на следующее обстоятельство: допуская существование разновидностей атомов одного и того же элемента, значительно отличающихся по величинам атомных весов, Крукс тем самым невольно ставил под сомнение определяющую роль этих величин в характеристике периодического изменения свойств элементов. Скажем, для атомов кальция с атомными весами 38 и 42 можно было бы a priori ожидать заметного различия в химических свойствах, ибо эти атомы сильно отличались по массе. Крукс, однако, на это обстоятельство практически не обратил внимания. [41]
Согласно теории переходных форм углерода, положенной в основу наших исследований, сочетание неодинаковых гибридных разновидностей атомов в единой полимерной структуре порождает множество аморфных форм этого вещества. [42]
 |
Построение периодической системы изотопов химических элементов. [43] |
Сложность построения периодической системы изотопов заключается в том, что она должна охватить около 1700 разновидностей атомов, тогда как в периодической системе элементов всего лишь 105 элементов или видов атомов. Форма системы изотопов играет решающую роль. Несмотря на то что предложен ряд вариантов клеточной системы изотопов ( О. Майтак и др.), ни один из этих вариантов не является наглядным и легко воспринимаемым. Более удачны системы в виде диаграмм, графиков и схем. [44]
Так как атомный вес элемента свинца ( а именно 207 2) представляет собой промежуточную величину между крайними значениями масс разновидностей атомов свинца, полученных в результате радиоактивного распада в различных семействах, то можно было думать, что природный свинец представляет собой смесь в определенной пропорции этих разновидностей по массе и атомный вес этого элемента - 207 2 - является результирующим из этой пропорции. [45]
Страницы: 1 2 3 4