Разность - термодинамический потенциал
Cтраница 1
Разность термодинамических потенциалов ( А - Анаб) берется в соответствии с уравнением ( 3) для оценки вкладов процесса обмена без учета изменения набухаемости. Поскольку величина ( АФ - АФнаб), или АФГ, близка по содержанию к свободной энергии обмена в безводной среде, можно думать, что процессы обмена ионов в безводной среде, если бы они были осуществимы экспериментально, характеризовались бы громадной избирательностью. Процессы такого рода, по-видимому, могут иметь место на границе газовой и твердой фаз. [1]
Если разность термодинамических потенциалов для каждого компонента в двух фазах равна нулю и если эти фазы находятся в контакте друг с другом или соединены таким образом, чтобы обеспечить молекулярный обмен между ними, то результирующий поток молекул ( и энергии) между обеими фазами для всех сортов молекул равен нулю. [2]
Эти градиенты и разности термодинамических потенциалов ( t, p, 6) являются силами, вызывающими соответствующие потоки тепла и влаги. К к В - коэффициент передачи соответственно тепла и влаги; EJ и Bq - показатель соответственно влаготепло - и тешювлагопередачи. Показатели тепловлаго - и влаготепло-проводности и передачи учитывают взаимное влияние явлений тепло - и влагообмена. [3]
Однако для использования разности термодинамических потенциалов и вторых вириальных коэффициентов для практической оценки качества растворителей требуется проведение специальных измерений термодинамических величин для каждой конкретной системы. [4]
Движущей силой диффузии является разность термодинамических потенциалов. [5]
Кинетическое уравнение (1.3) для разности термодинамических потенциалов фаз / отличается от (1.1), (1.2) тем, что величина / релаксирует не к нулевому, а конечному значению / е, представляющему плотность тепловой энергии, вводимой в систему. Отрицательная обратная связь величин и к Т с f означает уменьшение термодинамического фактора превращения с ростом скорости фронта кристаллизации и его температуры. Очевидно, это спадание является отражением принципа Ле-Шателье для рассматриваемой задачи. Действительно, взрывная кристаллизация обусловлена положительной обратной связью скорости и и термодинамического фактора / с температурой Т в уравнении (1.2), которая приводит к разогреву фронта кристаллизации, способствующему развитию неустойчивости. [6]
Движущей силой спекания является разность термодинамических потенциалов мелких и крупных частиц. [7]
Движущей силой спекания является разность термодинамических потенциалов мелких и крупных частиц. У первых, как известно, он выше за счет более высокой поверхностной энергии. По современным теориям, спекание, видимо, может осуществляться двумя механизмами: за счет диффузии частиц и за счет переноса атомов. Надежные экспериментальные доказательства спекания только по одному из механизмов отсутствуют, и, возможно, оба механизма могут действовать совместно. [8]
Движущей силой спекания является разность термодинамических потенциалов мелких и крупных частиц. [9]
Движущей силой диффузионного процесса является разность термодинамических потенциалов. Путем перераспределения вещества система стремится к выравниванию локальных разностей потенциалов, и, следовательно, стремится приблизиться к термодинамическому равновесию. Это выравнивание и осуществляется благодаря диффузии. [10]
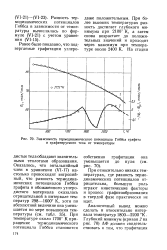 |
Зависимость термодинамического потенциала Гиббса графита и графитируемого тела от температуры. [11] |
При относительно низких температурах, где разность термодинамических потенциалов отрицательна, большую роль играют кинетические факторы и процесс графитообразования в твердой фазе практически не идет. [12]
Термодинамической мерой сродства между взаимодействующими компонентами является разность термодинамических потенциалов ( например, разность изобарио-изотермических потенциалов AG) при постоянных температуре и давлении. Чем больше абсолютная величина AG, тем полнее протекает процесс, тем больше сродство между компонентами. Процессы растворения сопровождаются уменьшением химических потенциалов. [13]
Термодинамической мерой сродства между взаимодействующими компонентами является разность термодинамических потенциалов ( например, разность изобарно-изотермически. [14]
Согласно (3.19) и (3.18), скорость реакции пропорциональна разности термодинамических потенциалов для исходного и переходного состояний. [15]
Страницы: 1 2 3