Равновесная разность - потенциал
Cтраница 2
Вследствие неодинаковой способности металлов к такому отделению ионов и различной гидратируемости ионов каждому металлу соответствует своя равновесная разность потенциалов и равновесная концентрация ионов в растворе. [16]
Но коль скоро мы при помощи проволоки из другого металла ( Си пли Pt), имеющего меньшую равновесную разность потенциалов с данною жидкостью, отведем часть лишних электронов / из цинка и жидкость ( черт. [17]
Если фазовая граница между двумя электролитами проницаема не для всех ионов, то на этой границе может установиться некоторая равновесная разность потенциалов. [18]
Здесь di - активность компонента i в растворе ( в стандартном растворе активность at 1); Е - равновесная разность потенциалов электрода из чистого компонента i и электрода - раствора, компонентом которого является i ( с активностью i, равной а -) в некотором растворе-электролите; F - число Фарадея; z - валентность иона i в растворе-электролите. [19]
 |
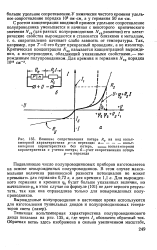
Семейство статических коллекторных характеристик триода в схеме с общей базой. [20] |
Область / / / называется областью насыщения и изображена на рис. 1 - 19 в сильно увеличенном масштабе, поскольку равновесная разность потенциалов на коллекторном переводе & Ф0к, к которой асимптотически стремятся характеристики при Ук0, составляет несколько десятых вольта, в то время как Vn 10 - т - 10а в. В области насыщения коллекторный и эмиттерный переходы смещены в прямом направлении. [21]
 |
Схема умножения. [22] |
Как следует из ( 101) и ( 106), с ростом концентрации примесей ( Nd и Afe) равновесная разность потенциалов q0 растет, а ширина перехода б падает. [23]
Важнейшей количественной характеристикой электрохимического элемента является электродвижущая сила ( ЭДС, обозначаемая в дальнейшем буквой Е), которая равна равновесной разности потенциалов между двумя полуэлементами. [24]
В случае замедленного разряда коэффициент переноса для одноэлектронного перехода равен отношению энергии активации электрохимического процесса w к электрохимической работе перехода заряженной частицы fq ( где F - число Фарадея, р - равновесная разность потенциалов), или, что то же, равен доле электродного потенциала, благоприятствующей протеканию катодного процесса. [25]
Итак, если, изучая диффузионные потенциалы, мы имели дело с неравновесными системами, где разность концентраций порождала постоянную направленную диффузию веществ, то доннанов потенциал представляет собой, в полном смысле слова, термодинамически равновесную разность потенциалов. Термодинамически равновесно и распределение концентраций между фазами доннановой системы. [26]
Однако в действительности, как только составлена электродная система, на границе раздела сразу же возникает потенциал, который возрастает до тех пор, пока не уравняются скорости обоих противоположных процессов А п Н2О А ( Н2О) П е и не установится равновесие. В этом случае возникает равновесная разность потенциалов 0 и нужно учитывать соответствующий электрический вклад в энергию системы. На левой части приведенного уравнения окислительно-восстановительной реакции это сказывается слабо, поскольку в ней фигурируют нейтральные компоненты. Эту энергию необходимо добавить к энергии частиц, фигурирующих в правой части уравнения реакции. [27]
Подавляющее число полупроводниковых приборов изготовляется на основе невырожденных полупроводников. В этом случае максимальная величина равновесной разности потенциалов не может превышать для германия 0 72 в, а для кремния 1 1 в. Для вырожденного германия и кремния ф0 будет больше указанных величин, но вычисление ф в этом случае по формуле ( 101) не дает верного результата, так как она справедлива только для невырожденных полупроводников. [29]
Возникновение равновесной разности потенциалов по сути своей аналогично установлению химического равновесия. Изучение закономерностей возникновения и изменения равновесной разности потенциалов составляет предмет электрохимической термодинамики. К области кинетики электрохимических реакций относится выявление отдельных стадий процесса и определение их скорости. Наряду с рассмотрением равновесных потенциалов важное значение приобретает исследование перенапряжения, возникающего при протекании тока через фазовую границу, что в общем равнозначно исследованию скорости химических реакций. [30]
Страницы: 1 2 3