Разогрев - реакционная смесь
Cтраница 2
Проведение обратимых экзотермических ХТП при оптимальной температуре в условиях отсутствия участков плавного разогрева реакционной смеси и перегрева ее выше ТОПт положительно сказывается на общей скорости процесса. В большинстве случаев эти факторы компенсируют снижение движущей силы процесса при протекании его в потоке полного смешения по сравнению с потоком идеального вытеснения. [16]
При этом происходит растворение цианида в течение 5 - Ю мин и разогрев реакционной смеси до 30 - 40 С. [17]
При втом происходит растворение цианида я течение 5 - Ю мни и разогрев реакционной смеси до 30 С. После охлаждения реакционной смеси образуется осадок ( Для соединений 2 3 осадок образуется только после пятидневной выдержки при комнатной температуре), который отфильтровывают, промывают водным изопропанолом, перекристаляи-зоаыаают из иаопропансла. Ниже приведена таблица с константами продуктов. [18]
Действие деструктирующих факторов наиболее заметно на начальной стадии реакции, во время разогрева реакционной смеси. В ходе реакции небольшое количество мономера выделяется за счет ацидолитического расщепления блокированных макромолекул. [19]
Некоторые авторы рекомендуют охлаждать кислоту и дистиллят перед очисткой с таким расчетом, чтобы последующий разогрев реакционной смеси не приводил к температуре, превышающей допустимый предел [51-53]; одновременно рекомендуется ограничить время контакта. [20]
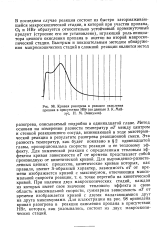 |
Кривая разогрева в реакции окисления. [21] |
Метод основан на измерении разности температур аТ между центром и стенкой реакционного сосуда, возникающей в ходе экзотермической реакции в результате разогрева реакционной смеси. Эта разность температур, как будет показано в § 2 одиннадцатой главы, пропорциональна скорости реакции и ее тепловому эффекту. Для химической реакции с определенным тепловым эффектом кривая зависимости аТ от времени представляет собой производную от кинетической кривой. При наличии двух макроскопических стадий, каждая из которых имеет свое значение теплового эффекта и свою область максимальной скорости, суммарная зависимость аТ от времени изображается кривой с двумя налагающимися друг на друга максимумами. Для иллюстрации на рис. 98 приведена кривая разогрева в реакции окисления пропана в присутствии НВг, которая, как указывалось, состоит из двух макроскопических стадий. [22]
Как указывалось выше, воспламенение реагента с окислителем может произойти не только в результате самоускорения реакции вследствие разветвления цепей, но и при наличии определенного теплового режима протекания реакции, приводящего к прогрессирующему разогреву реакционной смеси. [23]
Самовоспламенению органических веществ при контакте с окислителями предшествует ряд промежуточных реакций, которые начинаются г, обычных условиях и протекают с большой скоростью. В результате первоначального энергичного разогрева реакционной смеси инициируются последующие пред-пламенные реакции окисления, приводящие затем к самовоспламенению. [24]
Разделив второе уравнение на первое, получим линейное соотношение между х и Т: ( Т - Гн) ДТ С - хн), совпадающее с уравнением (4.120), выведенного для режима идеального вытеснения. Таким образом, разогрев реакционной смеси ( Т - Тн) не зависит от пути превращения - в режиме смешения или вытеснения. [25]
Понятие цепное воспламенение не следует смешивать с понятием теплового воспламенения. Последнее возникает в результате прогрессирующего разогрева реакционной смеси в результате сильно экзотермической реакции при недостаточно интенсивном теплоотводе ( подробнее см. § 3 гл. [26]
Так как скорость реакции образования 3-пентеновой кислоты из бутадиена значительно превосходит скорость ее гидрокарбоксилирования в бутандикарбоновые кислоты [1], в качестве исходного продукта использовался бутадиен. Считалось, что за время разогрева реакционной смеси до рабочей температуры бутадиен должен превращаться в 3-пентеновую кислоту. С другой стороны, незначительное образование бутандикарбоновых кислот к моменту вывода системы на нужный режим отмечалось только в опытах с повышенной температурой ( 210 и 220 С, опыты 57 и 63) и малой концентрацией воды ( опыт 14); в этих случаях вводилась поправка на время - аналогично описанному в предыдущей статье. [27]
Было решено использовать наиболее простой тип промышленного реактора - адиабатический. Однако из-за значительной величины ДГад ( разогрев реакционной смеси) целесообразно применять два последовательных адиабатических слоя катализатора с промежуточным охлаждением реакционной смеси холодным водородсодержащим газом. [28]
Реакция между сильной кислотой и основанием имеет ионный характер, протекает с большой скоростью, вследствие чего выделяющееся тепло не успевает рассеиваться. Это в свою очередь приводит к разогреву реакционной смеси и окислению всей молекулы. [29]
Цепное воспламенение не следует смешивать с тепловым воспламенением. Последнее возникает в сильно экзотермической реакции в результате прогрессирующего разогрева реакционной смеси при недостаточно интенсивном теплоотводе ( подробнее см. § 2 гл. Цепное воспламенение ( взрывное протекание процесса) является общим свойством всех цепных разветвленных реакций. [30]
Страницы: 1 2 3