Разрушение - комплекс
Cтраница 2
Разрушение комплексов и регенерация растворителя наиболее эффективно достигаются при использовании воды. [16]
Разрушение комплексов производят термически. [17]
Разрушение комплекса, образованного сераорганическим соединением с металлом, может происходить и без сольватации органических кислот на углеводородных радикалах присадки. Дело в том, что металл и масло в процессе испытаний нагреваются выше 140 С и подвергаются воздействию кислорода воздуха. При этом комплексы, находящиеся под воздействием силового поля металла, способны легко окисляться с отщеплением углеводородной их части. [18]
Разрушение гнефлуоресцирующих комплексов тяжелых металлов происходит лишь при действии более сильного, чем ЭДТА, комп-яексона - циклогександиаминтетрауксусной кислоты. [19]
Для разрушения комплекса А1С1Э смесь осторожно выливают на [ 25 г измельченного льда, добавляют немного конц. ОН) 3 н отделяют органическую фазу. Затем объеди - нные органические фазы промывают водой, 2 % - ным NaOH, снова юдой и насыщенным раствором NaCl. [20]
Для разрушения комплекса необходимо нагревание его со значительным количеством растворителя. В работе [1] разрушающие агенты ( растворители) разбиты на три группы: 1) растворяющие только углеводородный компонент комплекса, но не растворяющие карбамид ( бензол, бензин, изооктан и др.); 2) растворяющие только карбамид, но не растворяющие углеводородный компонент комплекса - это вода, а также водные растворы низших спиртов и карбамида; 3) растворяющие в той или иной степени как карбамид, так и нормальные алканы. [21]
Исследование разрушения комплексов, проводившееся при 10 - 80 С, позволило установить влияние на степень разрушения комплекса температуры и количества воды. Одновременно установлено влияние тех же факторов на выход н-парафинов при разрушении тех же образцов комплекса. [22]
Примерами разрушения комплексов могут служить реакции аммиакатов серебра, меди ( II) и кадмия с кислотами. [23]
Скорость разрушения комплекса и есть скорость одной из стадий реакции, и в многостадийных реакциях часто образуется несколько различных комплексов. [24]
Примерами разрушения комплексов могут служить реакции аммиакатов серебра, меди ( II) и кадмия с кислотами. [25]
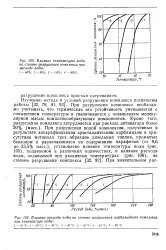 |
Влияние температуры воды на степень разрушения комплекса при расходе воды.| Влияние расхода воды на степень разрушения карбамидного комплекса при температуре воды. [26] |
При разрушении комплекса необходимо учитывать, что термическая его устойчивость уменьшается с повышением температуры и увеличивается с повышением молекулярной массы комплексообразующих компонентов. [27]
При разрушении комплексов или протонированных форм ( обычно это проводится путем выливания реакционной смеси в ледяную воду) выделяется смесь изомерных соединений, состав которой обычно не соответствует равновесному, поскольку катализатор при этом переходит в неактивное состояние вследствие гидратации. Таким образом, в этих условиях могут быть получены отдельные соединения или их смесь в соответствии с относительной термодинамической устойчивостью комплексов. При выделении веществ из реакционной смеси в чистом виде ( при перегонке или перекристаллизации) равновесие также сдвигается в сторону более легко кипящей формы или в сторону той формы, энергия кристаллизации которой больше. [28]
При разрушении комплекса цвет раствора изменяется от голубого до фиолетового. Этого времени достаточно для практически полного прохождения процесса, так как в дальнейшем увеличение оптической плотности соизмеримо с ошибкой ее измерения. С целью уменьшения растворимости определение ведут в 50 - 70 % - ном водно-ацетоновом или водно-спиртовом растворе. [29]
 |
Значения идеального коэффициента разцелзния в сиетеие халькогеноводород - примесь. [30] |
Страницы: 1 2 3 4