Коррозионное разрушение - сталь
Cтраница 2
Как показывают данные, приведенные в табл. IV.3, непрерывная дозировка АНПО в затрубное пространство скважины - приводит к торможению коррозионного разрушения стали. [16]
Подобная фиксация кислорода возобновляет процесс коррозии: участие в процессе твердого деполяризатора катодных участков объясняет часто встречающиеся на практике разнообразные формы коррозионных разрушений стали, например точечной, или булавочной, коррозии, которая за короткое время ( за 1 - 2 года) проникает через всю толщу металла труб толщиной 3 мм. Кислородная коррозия без участия оксидов железа ( III) в качестве переносчиков кислорода не может протекать с такой скоростью и в виде точечной формы, которая типична для совместного действия на металл указанных стимуляторов коррозии. [17]
В табл. 20.1 и 20.2 представлены результаты испытаний коррозионной стойкости металлов и сплавов в условиях альдольной конденсации масляного альдегида и концентрирования водных растворов этриола, которые проводились при температурах, не превышающих 60 С. Коррозионное разрушение сталей на указанных стадиях процесса определяется присутствием серной кислоты и масляного альдегида, в котором при длительном хранении на воздухе образуется масляная кислота. Данные по коррозионной стойкости материалов в масляной кислоте приведены в гл. [18]
Интенсивное развитие электрокоррозии стали в грунте под действием переменного тока наблюдается только при достижении определенного ( критического) значения поверхностной плотности переменного тока. В интервале плотностей тока утечки ниже критического значения коррозионные разрушения стали определяются в основном процессами почвенной коррозии. [19]
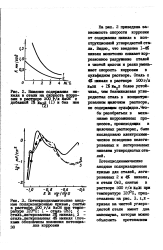
На рис. 2 приведена зависимость скорости коррозии от содержания никеля в конструкционной углеродистой стали. Видно, что введение I-4 & никеля монотонно снижает коррозионное разрушение сталей в чистой щелочи и резко уменьшает скорость коррозии в сульфидном растворе. Сталь с 4& никеля в растворе 500 г / л НаОН 1 % MagS более устойчива, чем безникелевая углеродистая сталь в концентрированном щелочном растворе, не содержащем сульфидов. Чтобы разобраться в механизме коррозионных процессов, происходящих в щелочных растворах, было исследовано электрохимическое поведение нелегированных и легированных никелем углеродистых сталей. [21]
Как видно из рисунков, в атмосфере азота под каплями воды не было заметных коррозионных разрушений стали, в то время как в атмосфере воздуха под каплями воды отмечена наиболее сильная коррозия. [22]
Ранее наиболее распространенными ингибиторами были формалин и уротропин, но в связи с их низкой эффективностью они стали применяться редко. В настоящее время широко распространен ингибитор уникол ПБ-5, который является липкой темно-коричневой жидкостью, обладающей хорошими защитными свойствами против коррозионного разрушения стали, способностью растворяться в соляной кислоте и не растворяться в воде - ни в пластовой, ни в минерализованной. Поэтому после нейтрализации кислоты с пластовым цементом уникол ПБ-5 выделяется из раствора в виде объемистой липкой органической массы в пористом пространстве пласта. Это, в свою очередь, приводит к ухудшению проницаемости пласта. Поэтому как сам ингибитор, так и ингибированная им кислота не пригодны для обработки полимик-товых коллекторов. [23]
Усталостное разрушение от действия напряжений обычно начинается с поверхности деталей. Количество повторяющихся циклов работы детали до образования усталостной трещины и характер разрушения определяются как величиной напряжений, так и интенсивностью процесса коррозии. Коррозионное разрушение сталей в условиях напряженного состояния деталей сложный и еще недостаточно изученный процесс. [24]
По программе совместных исследований с ВНИИнефтемашем были проведены длительные ( 2000 ч) испытания образцов на. На образцах из Ст Х18Н10Т было обнаружено поверхностное науглероживание, которое идет преимущественно по границам зерен аустенита и приводит к обеднению границ зерен хромом. Науглероживание провоцирует коррозионное разрушение стали в среде, содержащей сернистые соединения. [25]
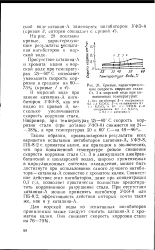 |
Кривые, характеризующие скорость коррозии стали Ст. 3 в морской воде при повышенных температурах. [26] |
Таким образом, проанализировав результаты всех вариантов испытания ингибиторов катапина - А, УФЭ-8, ПБ-8 / 2 с хроматом калия, мы приходим к заключению, что при повышенной температуре резкое снижение скорости коррозии стали Ст. А совместно с хроматом калия. Совместное действие этих ингибиторов, даже при концентрации 0 1 г / л, позволяет практически полностью предотвратить коррозионное разрушение стали. При отсутствии катапина - А можно применять ингибитор УФЭ-8 или ПБ-8 / 2, эффективность действия которых почти такая же, как и у катапина - А. [27]
Не полностью используемый бактериями на окислительные процессы кислород обеспечивает протекание катодной деполяриза-ционной реакции грунтовой коррозии стали в анаэробных условиях. Сероводород уменьшает перенапряжение водорода в кислых и слабокислых грунтах, облегчая протекание катодного процесса в этих условиях. Сульфид-ионы, действуя как депассиваторы, а также связывая железо в труднорастворимые и малозащитные сульфиды, растормаживают анодный процесс коррозии стали. По данным некоторых исследователей, скорость коррозионного разрушения стали при воздействии этих бактерий может возрастать в 20 раз. [28]
Как видно из представленных зависимостей комбинированное покрытие ( кривая 2) полностью блокирует поверхность стали и коррозия в широкой области потенциала не происходит. В тоже время сталь без покрытия ( кривая 1) начинает растворяться при потенциале близком к нулю и при дальнейшей поляризации плотность анодного тока имеет тенденцию к увеличению, т.е. сталь в солевом растворе химически активна, за исключением области в интервале 0 7 - 0 9 В, где наблюдается частичное торможение. Плазменное покрытие ( кривая 2) защищает сталь вплоть до 0 5 В. Однако, при дальнейшей поляризации покрытие не препятствует коррозионному разрушению стали. Очевидно, это связано с тем, что плазменное покрытие вследствие высокой пористости сохраняет доступ электролита. Комбинированное покрытие, как и в случае 5 % раствора НС1, эффективно защищает сталь. [29]
Низкоуглеродистые стали на чистом воздухе при относительной влажности, несколько превышающей критическую, корродируют незначительно, поскольку коррозия замедляется при образовании начального слоя ржавчины. Годовая скорость коррозии не-превышает 0 005 мм. В промышленной среде в таких же условиях она значительно выше и достигает 0 008 - 0 12мм вследствие наличия загрязнений воздуха, главным образом двуокиси серы ш пыли. Двуокись серы поглощается пылью и, вступая в реакцию с-водой и кислородом, образует серную кислоту, которая увеличивает коррозионное разрушение стали. [30]
Страницы: 1 2 3