Разрыв - растворимость
Cтраница 1
Разрыв растворимости при температуре 1300 имеет место при содержании 16 - 30 мол. [1]
Если разрыв растворимости достигает области перехода в жидкое-состояние, как на рис. 107, прежнее двухфазное равновесие менаду жидкостью и твердым раствором непрерывного ряда переходит в два новых двухфазных равновесия, в каждом из которых представлены попрежнему жидкость и один из твердых растворов распада. [2]
Мо имеет место разрыв растворимости в жидком состоянии. [3]
С существует область разрыва растворимости. Данные работы [2] допускают существование области разрыва растворимости при температурах ниже 100 С. Максимальные значения растворимости равны соответственно 41 7 и 38 0 % ( ат. В обоих случаях наблюдается логарифмическая зависимость равновесного давления от температуры. [4]
Разберем случай, когда разрывы растворимости в области непрерывного ряда твердых растворов возникают во всех трех двойных системах и распространяются при более низких температурах в тройной системе с образованием трехфазного разрыва растворимости. [6]
 |
Марки и основные характеристики монокристаллов GaP. [7] |
Противоречивы сведения о существовании разрывов растворимости в системе GaAs - QaSb. Фазовые диаграммы наиболее изученных псевдобинарных систем показаны на рис. 20.34. Поскольку соединения - партнеры кристаллизуются в одной и той же структуре цинковой обманки, то для твердых растворов, как правило, выполняется закон Вегарда, предусматривающий линейное изменение периода кристаллической решетки в зависимости от состава. [8]
При повышении температуры область разрыва растворимости в тройной системе постепенно сужается ( рис. 82), пока, наконец, не превращается в точку на стороне АВ при температуре, отвечающей критической точке ko в этой двойной системе. [9]
Рассмотрим вначале случай, когда эвтектический разрыв растворимости возникает в одной из двойных систем, тогда как в двух других CS. [10]
 |
Диаграмма вертикального разреза III.| Диаграмма вертикального разреза IV. [11] |
Вначале рассмотрим случай, когда перитектический разрыв растворимости возникает в одной из двойных систем, тогда как в двух других системах компоненты образуют непрерывный ряд твердых растворов. Диаграмма состояния, отвечающая этому случаю равновесия, показана на рис. 139 в перспективном изображении и на рис. 140 - в проекции на концентрационный треугольник. [12]
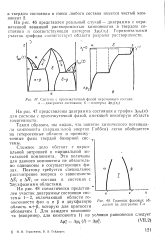 |
Система с промежуточной фазой переменного состава. а - диаграмма состояния. б - изотерма ДЦ2 ( 2. [13] |
Горизонтальный участок графика соответствует области разрыва растворимости. [14]
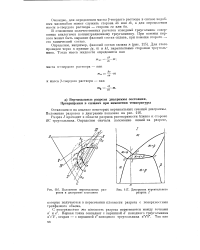 |
Положение вертикальных разрезов в диаграмме состояния.| Диаграмма вертикального разреза. [15] |
Страницы: 1 2 3 4 5
