Разрыв - растворимость
Cтраница 4
Подобный переход будет, очевидно, иметь место в том случае, когда в одной из двойных систем наблюдается эвтектический разрыв растворимости, в другой - перитектический. Обсуждению этого случая посвящен следующий раздел. [46]
На диаграмме таяния - плавления системы с разрывом взаимной растворимости в жидком состоянии ш при отсутствии молекулярного соединения в области разрыва растворимости кривая таяния следует вдоль эвтектической горизонтали, в то время как кривая плавления, в соответствии с рис. 218 ( стр. При наличии молекулярного соединения, плавящегося с образованием двух жидких фаз, кривая плавления состоит, соответственно рис. 219 ( стр. Кривая таяния и в этом случае указывает на состав соединения. Она падает от точки таяния компонента А до первой эвтектической горизонтали, идет вдоль нее, минуя эвтектическую точку, почти до ординаты молекулярного соединения, затем поднимается к точке, соответствующей температуре плавления соединения, непосредственно от нее вновь круто падает ко второй эвтектической горизонтали, идет вдоль последней, проходя через вторую эвтектическую точку, и круто поднимается к точке таяния компонента В. В обоих случаях по полученной кривой можно попутно определить растворимость обеих жидких фаз и критическую температуру растворения. [47]
На диаграмме таяния - плавления системы с разрывом взаимной растворимости в жидком состоянии 114 при отсутствии молекулярного соединения в области разрыва растворимости кривая таяния следует вдоль эвтектической горизонтали, в то время как кривая плавления, в соответствии с рис. 218 ( стр. При наличии молекулярного соединения, плавящегося с образованием двух жидких фаз, кривая плавления состоит, соответственно рис. 219 ( стр. Кривая таяния и в этом случае указывает на состав соединения. Она падает от точки таяния компонента А до первой эвтектической горизонтали, идет вдоль нее, минуя эвтектическую точку, почти до ординаты молекулярного соединения, затем поднимается к точке, соответствующей температуре плавления соединения, непосредственно от нее вновь круто падает ко второй эвтектической горизонтали, идет вдоль последней, проходя через вторую эвтектическую точку, и круто поднимается к точке таяния компонента В. В обоих случаях по полученной кривой можно попутно определить растворимость обеих жидких фаз и критическую температуру растворения. [48]
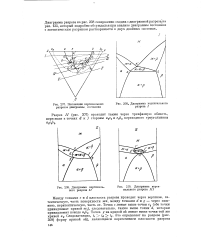
Естественно, что монотектическое и синтектическое трехфазные равновесия вносят самостоятельный элемент в общую картину фазового равновесия двухкомпонентной системы, отличающейся разрывом растворимости в жидком состоянии, поскольку они завершаются стабилизацией либо одного ( рис. 56 а), либо двух ( рис. 56 6) двухфазных равновесий с участием жидких фаз, способных при дальнейшем охлаждении кристаллизоваться и, следовательно, формировать другие трехфазные равновесия - уже эвтектического либо перитектического типа. [50]
 |
Положение вертикальных разрезов диаграммы состояния.| Диаграмма вертикального разреза.| Диаграмма вертикального разреза II.| Диаграмма вертикального разреза III. [51] |
Диаграмма разрезана рис. 208 совершенно сходна с диаграммой разрезала рис. 135, который подробно обсуждался при анализе диаграммы состояния с эвтектическим разрывом растворимости в двух двойных системах. [52]
 |
Проекция диаграммы. [53] |
Так как компоненты А ж В, так же как А т С, по условию неограниченно смешиваются в твердом состоянии, эвтектический разрыв растворимости должен замыкаться внутри диаграммы. [54]
 |
Диаграмма состояния с пери-тектическим разрывом растворимости в одной из двойных систем.| Проекция диаграммы. [55] |
Поскольку компоненты Л и Б, так же как и компоненты А и С, по условию неограниченно смешиваются в твердом состоянии, перитектический разрыв растворимости должен замыкаться внутри тройной диаграммы состояния. [56]
В работах [1-3] была установлена неограниченная смешиваемость иттрия и неодима в жидком состоянии, образование непрерывного ряда твердых растворов высокотемпературными кубическими модификациями и наличие разрыва растворимости с образованием промежуточной б-фазы в области стабильности низкотемпературных гексагональных модификаций этих металлов. [57]
Нижняя часть диаграмм, образующих циркониевый угол системы, повторяет верхнюю: в системе цирконий - титан существует непрерывный ряд а-твердого раствора, в системе цирконий-молибден-эвтектоидный разрыв растворимости. Политермические разрезы Mo: Ti 4: l; 1: 1; 1: 4 ( рис. 2) очень хорошо показывают переход от системы цирконий-молибден с эвтектикой и эвтектоидом к системе цирконий-титан с непрерывным рядом твердых растворов в р - и а-модификациях. В разрезе Mo: Ti 4: 1 ( рис. 2, а ] границы солидуса и ликвидуса нанесены из теоретических соображений, однако экстраполяция линий растворимости для р-твердого раствора циркония выше 1300 показывает, что в этом разрезе так же, как и в системе цирконий-молибден, существует ограниченная растворимость компонентов в р-фазе циркония. В разрезе Mo: Ti 1: 1 при температурах выше 1100 вплоть до солидуса существует непрерывный ряд р-твердых растворов, в нижней части сечения сохраняются области, связанные с эвтектоидным распадом р-твердого раствора. [58]
Поверхности растворимости выделяют двухфазную область разрыва растворимости а Л, ограниченную со стороны граней призмы их частями a1b1b ( a 0a1 и abb a а, представляющими разрыв растворимости в двойных системах, сверху-поверхностью а [ 3 трехфазного объема и снизу - частью а ЬЬ йа йа основания призмы. [59]
Точно так же, если смесь еще не закристаллизовалась ( не замерзла), наблюдается нижняя критическая температура растворения - достаточно низкая температура, при которой также исчезает разрыв растворимости. [60]
Страницы: 1 2 3 4 5
