Разрыв - связь
Cтраница 1
Разрыв связи С - Р в со единениях ( 2 3) происходит и при пропускании сухого хлористого водорода через их раствор в бензоле уже при комнатной тем-пературе, при этом образуются соль индолина ( 7) и треххлорис-тый фосфор. [1]
Разрыв связи С-С в натриевой соли нитробензальфталида происходит также при действии брома, но тогда образуется фенилдибромннтрометан. [2]
Разрыв связи С - Н с образованием метил-аниона и протона осуществиться не может, так как только на превращение атомарного водорода в протон ( Н - - Н) в газовой фазе требуется 1305 кДж / моль. [3]
Разрыв связей без растяжения волокна приводит к укладке цепей в свер Хюокращенную форму, и не исключено, что в направлении, перпендикулярном плоскости основного зигзага, возникает упорядоченность, соответствующая водородным связям. [4]
Разрыв связей между частицами при дроблении происходит по разным узлам решетки кристаллов. Разрушение кристаллической решетки приводит к появлению избыточных электрически заряженных ионов. Это особенно заметно при тонком измельчении кристаллических веществ и материалов. Все это обусловливает увеличение химической активности свежеобразованной поверхности. [5]
Разрыв связей С-С не представляет большого интереса для целей органического синтеза. При термическом воздействии эти связи разрываются лишь при температурах, близ шх к8000, что существенно только для некоторых реакций крекинга. Если разрыв облегчается вследствие резонанса между возможными радикалами, то последние часто слишком устойчивый в результате недостаточно реакционноспособны, чтобы их можно было использовать в качестве промоторов. Примером могут служить гексаарилэтаны, изученные Гомбергом. Для этих молекул уже при обычной температуре наблюдается диссоциация на триарилметильные радикалы ( а), приводящая к истинному равновесию; диссоциация усиливается при наличии пространственных затруднений, препятствующих возвращению к исходной форме, как в случае гекса - ( о-толил) - этана. [6]
Разрывы связей между атомом углерода и гетероатомом часто используются для получения свободных органических радикалов. Эти разрывы осуществляются чаще всего с помощью металлов, способных к отдаче одного из неспаренных электронов с внешней электронной оболочки. [7]
Разрыв связи при флуктуационном удлинении можно моделировать локальным тепловым расширением, которое также связано с ангармонизмом. [8]
Разрыв связей происходит лишь между атомами или группами, непосредственно примыкающими к активным центрам. В результате перераспределения связи как бы поворачиваются, образуя новые соединения. Эти схемы очень наглядно изображают поверхностные реакции. [9]
Разрыв связи С-С происходит между углеродными атомами где-то вдоль цепи, что ведет к образованию молекул алкена и алкана с более низкими молекулярными весами, чем у исходного алкана. [10]
Разрыв связи с ядром и выражает собой возможное структурное превращение. Разрыв наступает, как только скорость частицы достигает некоторого уровня, определяемого указанным равновесием. [11]
Разрыв связей предпочтительнее осуществляется у места разветвления в углеродной цепи. Остальная часть спектра очень сходна со спектрами длинноцепочечных углеводородов, за исключением того, что пики, соответствующие ионам С5, обладают повышенной интенсивностью ( благодаря отрыву цепи C2i), а пики, соответствующие ионам С4 - несколько пониженной интенсивностью. Ионы 21 не обладают значительной распространенностью. Это обычно наблюдается в случае длинных ответвлений, причем положительный заряд редко остается на таком осколке. Плавная кривая, полученная при графическом рассмотрении зависимости интенсивности ионов CnH2n i от числа углеродных атомов для к-пара-финовых углеводородов, нарушается в случае разветвленных парафиновых углеводородов с высоким молекулярным весом в точках, соответствующих отщеплению каждого ответвления углеродной цепи. Например, в масс-спектре 11-неопентилгенэйкозана [ ( С10Н21) 2СНСН2 - С ( СН3) з ], который приведен на рис. 135, имеются значительные пики в области массовых чисел С25, С22, С2Ь С16, Ci3, С12, соответствующих отрыву 1, 4, 5, 10, 13 и 14 углеродных атомов. [12]
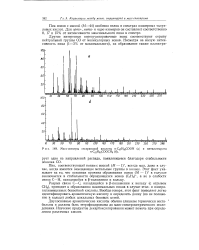 |
Масс-спектры стеариновой кислоты н - С НзсСООН ( а и метилстеаратз. [13] |
Разрыв связи С-С, находящейся в Р - положении к кольцу ( с отрывом СН3), приводит к образованию максимальных пиков в случае этил - и изопро-пилзамещенных бензойной кислоты. Вообще говоря, этот факт позволяет легко идентифицировать ароматическую кислоту и определить длину ( но не положение в кольце) любых алкильных боковых цепей. [14]
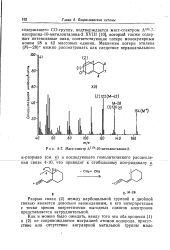 |
Масс-спектр Д1 9 - 10-метилокталона - 2. [15] |
Страницы: 1 2 3 4