Разрыхление - поверхность
Cтраница 2
Аналогичную трактовку допускают также результаты Рогинского, Третьякова и Шехтер [3], наблюдавших интенсивное разрыхление поверхности железа, меди и платины при проведении реакции разложения аммиака. При обработке катализатора равновесной смесью разрыхление происходит значительно медленнее. Еще менее заметен этот эффект при обработке образцов отдельными компонентами реакционной смеси - азотом или водородом. [16]
При исследовании осаждения металлов нужно учитывать, что при многократном осаждении - растворении металлов происходит разрыхление поверхности электрода, которая не восстанавливается после анодного растворения металла; кривые ф - t становятся размытыми, переходы от одного участка к другому нечеткими. По данным [368] наиболее удобными яв-ляются катоды из молибдена, вольфрама или платины. При высоких температурах ( 700 С) срок службы таких катодов ограничен 3 - 5 циклами. [17]
Согласно этой теории, появление анодного эффекта связано с выделением на аноде галоида ( фтора), который вызывает разрыхление поверхности угольного анода с образованием пылевидного углерода. Действие окиси алюминия, содержащейся в электролите, заключается в том, что выделяющийся на аноде кислород сжигает углеродистую пыль на поверхности анода и тем самым препятствует возникновению анодного эффекта. [18]
Длительная поляризация титан-двуокисномарганцевых анодов в сульфат-хлоридных электролитах показала, что толщина анодного покрытия видимо не изменяется, а наблюдается незначительное разрыхление поверхности окисла. [19]
Таким образом, увеличение скорости коррозии при катодной поляризации может быть обусловлено снижением степени окисленности образца, а также разрыхлением поверхности при наво-дороживании. [20]
Одновременно наблюдается увеличение емкости двойного слоя от - 25 до - 250 мкФ / см2, что указывает, по-видимому, на разрыхление поверхности. Следовательно, условия измерений также влияют на значения кинетических параметров. В табл. 11 сопоставлены кинетические характеристики этой реакции на различных углеродных электродах и платине. [22]
Выделение GeH4 с поверхности катода или реакция АзНз и 8ЬНз с ионами As и Sb, находящимися в растворе, приводит к разрыхлению поверхности цинка. [23]
Поверхностно-активные вещества типа мыл ионоген-ные и неионогенные), снижая поверхностное натяжение на границе вода - мономер, способствуют лучшему диспергированию ви-нилхлорида, разрыхлению поверхности образующихся частиц, повышению их пористости. [24]
В присутствии тех добавок, которые уменьшают разрушение свинцовых анодов при электролизе, разрыхление поверхности меньше, а в присутствии иона С1 -, разрыхление поверхности увеличивается. [25]
Удалось показать, что самоускорение реакции не является результатом удаления с поверхности покрывающих или отравляющих ее примесей, а происходит благодаря явлению автокатализа, который наблюдается вследствие разрыхления поверхности контакта и создания высокоактивных поверхностных структур за счет энергии первичной экзотермической реакции. [26]
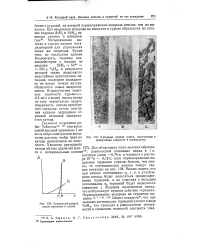 |
Катодные осадки цинка, полученные в присутствии германия в электролите.| Совместный разряд, ионов германия и цинка. [27] |
Перенапряжение водорода на германии высокое 16 - 17 31 31 ( 3 - Опыты показали31, что при высоких потенциалах германий улетает в виде GeH4, что приводит к разрыхлению поверхности и снижению истинной плотности тока. [28]
Констейбл показал, что каталитически активная медь может быть получена: а) пропусканием над медной сеткой аммиака при 820 С, причем в результате разложения аммиака и частичного образования нитрида меди происходит сильное разрыхление поверхности металла; б) быстрым восстановлением солей меди и СиО моноксидом углерода; в) термическим разложением медных солей одноосновных жирных кислот. [29]
Дальнейшее насыщение растворов с целью получения концентраций, необходимых для переработки сернокислого раствора, до продукта соответствующей реактивной квалификации приводит к тому, что наряду с переходом ионов родия в раствор происходит процесс разрыхления поверхности электрода, обусловленный обратным процессом выделения родия на электроде в отрицательный полупериод переменного тока. При этом рост концентрации соли в растворе практически прекращается. [30]
Страницы: 1 2 3 4
