Разряд - ион - натрий
Cтраница 1
Разряд ионов натрия да твердом катоде происходить не может, так как для его протекания необходим значительно более отрицательный потенциал, чем потенциал выделения водорода. [1]
Разряд ионов натрия из водных растворов на твердом катоде невозможен вследствие более высокого потенциала их разряда по сравнению с водородом. Поэтому остающиеся в растворе гидро-ксильные ионы образуют с ионами натрия раствор щелочи. [2]
Потенциал разряда ионов натрия имеет более положительное значение, чем обратимый потенциал атрия, за счет образования амальгамы и непрерывного отвода ее с поверхности вследствие растворения в избытке ртути. [3]
 |
Оксидно-рутениевый анод.| Устройство для опускания графитового анода. [4] |
Процесс разряда ионов натрия происходит no - существу на амальгамном электроде, причем концентрация натрия в амальгаме постепенно увеличивается от места подачи в электролизер ртути до места вывода амальгамы. [5]
На жидком катоде разряд ионов натрия заметно облегчается за счет деполяризации при образовании сплава. Если основной металл ( Pb, Cd, Sn) содержит примеси висмута, то при катодном выделении щелочного металла образуется интерметаллическое соединение Na3Bi с высокими температурой плавления и теплотой образования. Поэтому образующийся интерметаллид плохо растворим в свинце и он может переходить в расплавленный едкий натр. [6]
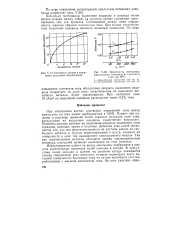 |
Активность натрия в амальгамах различной концентрации.| Зависимость потенциала. [7] |
Поскольку потенциалы выделения водорода и разряда ионов натрия близки между собой, на ртутном катоде протекают одновременно оба эти процесса. Соотношение между ними определяется главным образом плотностью тока. При малых плотностях тока выделение водорода является основным процессом. [8]
 |
Зависимость выхода по току от плотности тока. [9] |
Избыток фтористого алюминия уменьшает вероятность разряда ионов натрия на катоде и снижает температуру плавления электролита, но значительно увеличивает его летучесть. Кроме того, в электролит вводят небольшие добавки MgF2 или Сар2, снижая тем самым температуру плавления электролита и растворимость алюминия в электролите, а следовательно, увеличивая выход по току. Слишком кислые электролиты также снижают выход по току. [10]
Гульдни неправильно объясняет катодный процесс разрядом ионов натрия с последующим химическим восстановлением свинца. В рассматриваемом случае, когда катодом служит элсктрошюпроводяпптйРЬЗ, находящийся под катодным потенциалом, следует считать первичным процесс восстановления ионов свинца в решетке PbS. Эквивалентное количество ионов S - - при этом освобождается из решетки сульфида и переходит в раствор, чем и объясняется дальнейшее анодное выделение серы. Мне нагнется, что такой механизм катодного процесса правильнее объясняет наблюдаемые явления. [11]
Следовательно, катодный процесс состоит в разряде ионов натрия с образованием жидкой амальгамы натрия. На катоде устанавливается равновесие не между ионами натрия и металлом натрия, а между ионами натрия и амальгамой, бедной по содержанию натрия. [12]
 |
Принципиальная схема ванны с ртутным катодом. [13] |
Амальгама натрия в электролизере образуется при разряде иона натрия на ртутном катоде. Катодом в электролизере служит амальгама. [14]
Однако это не так, и скорость разряда ионов натрия значительно выше скорости разряда ионов водорода. Это происходит из-за большого перенапряжения водорода на ртутном катоде. [15]
Страницы: 1 2 3 4