Разряд - металлический ион
Cтраница 1
Разряд металлических ионов обладает достаточной скоростью, а кристаллизация металлов при электролизе является наиболее замедленной стадией. [1]
Разряд металлических ионов обладает достаточной скоростью, а кристаллизация является замедленной стадией. При этом образование двумерного зародыша кристалла является наиболее замедленным процессом. [2]
Перенапряжение при разряде металлических ионов, а также в случае выделения кислорода при окислительно-восстановительных реакциях, как правило, подчиняется уравнению Тафеля. Это свидетельствует о том, что причины перенапряжения всех упомянутых реакций аналогичны. Реакция же рекомбинации в большинстве перечисленных процессов отсутствует. [3]
В противоположность водороду разряд металлических ионов Zn2 сопровождается незначительной поляризацией. [4]
Химическая поляризация при разряде металлических ионов может достигать очень больших значений ( свыше 1 в. Наличие сплошной адсорбционной пленки приводит к очень низким значениям предельного тока, возрастающего при приближении к потенциалу десорбции адсорбированных веществ с поверхности электрода. Авторы считают, что при проникновении ионов через адсорбционную пленку происходит значительная деформация последней и что существо тормозящего действия добавок сводится к наличию значительных сил отталкивания между подходящими к электроду ионами и молекулами адсорбционного слоя. [5]
 |
Схема установки для измерения емкости. [6] |
Новые данные для процесса разряда металлических ионов, полученные по этому методу, не были до сих пор опубликованы, хотя некоторые из них сообщались на Киевской конференции 1948 г. Эти данные будут приведены в настоящем докладе. Поскольку сам метод переменного тока описан в литературе [1], здесь он будет изложен только схематически. [7]
 |
Принципиальная схема установки для хромирования. [8] |
В результате этой реакции происходит разряд металлических ионов на поверхности детали. [9]
 |
Рассчитанные по уравнению ( 8. [10] |
Для определения изменений, вносимых адсорбцией органических веществ в кинетику разряда металлических ионов, необходимо знать кинетические параметры протекания этого процесса в чистом, не содержащем органических добавок электролите. [11]
Недавно нами [7] было показано, что производный полярографический спектр разряда металлических ионов легче получить, чем обычный. На рис. 5 приведены производная и обычная подпрограммы для раствора, содержащего ионы кобальта, свинца, кадмия, водорода, алюминия и натрия. В то время как па обычной полярограмме ясно выраженный диффузионный ток наблюдается только у кобальта, а диффузионные токи свинца, кадмия и водорода сливаются в одну общую волну, па производной полярограмме этого же электролита имеются четкие токи всех катионов, концентрация которых в электролите мала. [12]
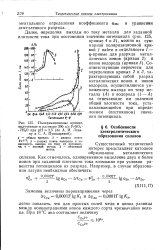 |
Поляризационные кривые, полученные ъ растворе 200 г / л FeSO4 7Н2О при. рН 2 5 ( по А. И. Левину и С. А. Пушкаревой. [13] |
Соответствующие пересчеты для определения кривых 2 и 3, характеризующих собой разряд металлических ионов и ионов водорода, осуществляются умножением выхода по току металла ( А) и водорода ( 1 - А) на отвечающие им значения общей плотности тока, устанавливающейся при определенном ( постоянном) значении потенциала. [14]
Соответствующие пересчеты для определения кривых 2 и 3, характеризующих собой разряд металлических ионов и ионов водорода, осуществляются умножением выхода по току металла ( А) и водорода ( 1 - А) на отвечающие им значения общей плотности тока, устанавливающейся при определенном ( постоянном) значе-нии потенциала. [15]
Страницы: 1 2 3